时间:2017-03-05 14:15:56
1、选择题 下列说法中,正确的是.
A.氢气在氯气中燃烧发出蓝色火焰
B.饱和氯水长期放置,颜色逐渐变浅
C.燃烧反应一定要有氧气参加
D.光照氯水有气泡冒出,该气体是氯气
参考答案:B
本题解析:H2在Cl2燃烧产生苍白色火焰.燃烧不一定有O2,如H2在Cl2中燃烧.D中放出的是O2.
本题难度:困难
2、选择题 有镁和铝的混合物粉末溶于4 mol・L-1的盐酸500 mL中,若加入2 mol・L-1的NaOH溶液,使产生的沉淀质量最大,则需加入NaOH的体积为
A.100 mL
B.500 mL
C.1 000 mL
D.1 500 mL
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列事实可证明氨水是弱碱的是
A.氨水能被弱酸醋酸中和
B.铵盐受热易分解
C.氨水可以使酚酞试液变红
D.0.1mol / L氯化铵溶液的pH约为5
参考答案:D
本题解析:A和C只能说明氨水显碱性,铵盐的热稳定性和氨水的弱碱性是无关的。D中溶液显酸性,说明氯化铵水解显酸性,越弱越水解,因此氨水属于弱碱。答案选D。
本题难度:一般
4、选择题 25℃时,有c(CH3COOH)+c(CH3COO-)=" 0." 1 mol・L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是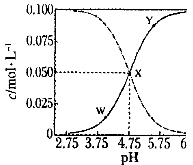
A.X点所表示的溶液中:c(Na+)+ c(OH-) = c(CH3COO-) + c(H+)
B.W 点所表示的溶液中:c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=" 0." 1mol・L-1
C.该温度下醋酸的电离平衡常数为10-4.75 mol・L-1
D.向X点所表示的溶液中加入等体积的0. 05mol・L-1NaOH溶液:c(H+)= c(CH3COOH)+c(OH-)
参考答案:C
本题解析:试题分析:A、根据图像可知,X点溶液显酸性,则根据电荷守恒可知c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),选项A不正确;B、W点溶液显酸性,同样根据电荷守恒可知 c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),所以c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=2 c(CH3COOH)<0.1mol/L,B不正确;C、该温度下醋酸的电离平衡常数=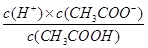 ,则根据X点的pH可知,该温度下醋酸的电离平衡常数为10-4.75 mol/L,选项C正确;D、向X点所表示的溶液中加入等体积的0. 05mol・L-1NaOH溶液,醋酸恰好反应生成醋酸钠,即溶液是醋酸钠溶液,所以根据质子守恒可知c(OH-)= c(CH3COOH)+ c(H+),D不正确,答案选C。
,则根据X点的pH可知,该温度下醋酸的电离平衡常数为10-4.75 mol/L,选项C正确;D、向X点所表示的溶液中加入等体积的0. 05mol・L-1NaOH溶液,醋酸恰好反应生成醋酸钠,即溶液是醋酸钠溶液,所以根据质子守恒可知c(OH-)= c(CH3COOH)+ c(H+),D不正确,答案选C。
考点:考查电离平衡常数的有关判断和计算、溶液中离子浓度大小比较
本题难度:一般
5、选择题 在某透明的强酸性溶液中,能大量共存的无色离子组是
A.K+、Na+、Cu2+、SO42-
B.Na+、Al3+、Cl-、NO3-
C.Na+、K+、CO32-、Cl-
D.K+、SO42-、Cl-、Ba2+
参考答案:B
本题解析:分析:强酸性溶液中存在大量的H+,离子之间不能结合生成气体、水、沉淀、弱电解质等,则离子能大量共存,并注意离子的颜色来分析,以此来解答.
解答:A.该组离子之间不反应,能共存,但Cu2+在溶液中为蓝色,与无色溶液不符,故A不选;
B.该组离子之间不反应,能共存,且离子均为无色,故B选;
C.因H+、CO32-结合生成水和气体,则不能共存,故C不选;
D.因SO42-、Ba2+能结合生成硫酸钡沉淀,则不能共存,故D不选;
故选B.
点评:本题考查离子的共存,明确信息及离子之间的反应即可解答,学生应熟悉复分解反应发生的条件来解答,题目较简单.
本题难度:简单