时间:2017-03-05 14:09:42
1、选择题 将15.6 g Na2O2和5.4 g Al同时放入一定量的水中,充分反应后得到200 mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72 L,若反应过程中溶液的体积保持不变,则( )
A.反应过程中得到6.72 L的气体(标况)
B.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
C.最终得到7.8 g的沉淀
D.最终得到的溶液中c(NaCl)=0.15 mol/L
参考答案:C
本题解析:15.6 g Na2O2和5.4 g Al的物质的量都是0.2mol,0.2mol过氧化钠可以生成0.1mol乙炔和0.4mol氢氧化钠。0.2mol铝消耗0.2mol氢氧化钠生成0.3mol氢气,即气体是0.5mol。6.72L氯化氢是0.3mol,其中0.2mol中和剩余的氢氧化钠,另外0.1mol和偏铝酸钠反应生成0.1mol氢氧化铝沉淀。此时溶液中还剩余0.1mol偏铝酸钠以及生成的0.3mol氯化钠,则溶液中钠离子的浓度是0.4mol÷0.2L=2.0mol/L。剩余只有选项C是正确的,答案选C
本题难度:一般
2、选择题 设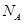 为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是
A.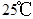 时,1g水中约含有6.02×1013个OH-
时,1g水中约含有6.02×1013个OH-
B.在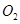 参与的反应中,
参与的反应中,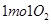 作氧化剂时得到的电子数一定是
作氧化剂时得到的电子数一定是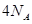
C.1.8g重水(D2O)中含NA个质子和NA个中子
D.标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA
参考答案:A
本题解析:A、水为中性,C(OH?)=1×10-7mol?L?1, 1g水为0.001L,含OH?:0.001L×1×10-7mol?L?1×6.02×1023=6.02×1013,正确;B、1molO2与Na在加热条件下反应生成Na2O2,得电子数为2NA,错误;C、1.8g重水(D2O)中含质子:1.8g÷20g/mol×10 ×NA,错误;D、辛烷在标准状况下为液体,不能用22.4L/mol,错误。
本题难度:一般
3、选择题 混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为0.821g/L,则混合气体中N2和CH4的体积之比为
A.1:1
B.1:4
C.4:1
D.1:2
参考答案:B
本题解析:混合气体在标准状况下的密度为0.821g/L,则混合气体平均相对分子质量是0.821×22.4=18.4。根据十字交叉法可知,混合气体中N2和CH4的体积之比为 ,所以答案选B。
,所以答案选B。
本题难度:一般
4、选择题 1molCO与1molCO2具有相同的 ( )
A.分子数
B.氧原子数
C.质子数
D.质量
参考答案:A
本题解析:根据阿伏加德罗定律可知物质的量相等的CO和CO2具有相同的分子数。答案选A。
考点:阿伏加德罗定律:
点评:本题根据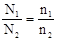 来判断,非常简单基础。
来判断,非常简单基础。
本题难度:一般
5、选择题 阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是
A.1 L 1 mol?L-1的HAc溶液中含有氢离子数约为6.02×1023
B.18 g D2O(重水)完全电解,转移的电子数约为6.02×1023
C.标态下,22.4L NO2气体,所含氧原子数约为2×6.02×1023
D.标态下,14g乙烯和丙烯的混合物中,含有共用电子对数目约为3×6.02×1023
参考答案:D
本题解析:A、醋酸是弱酸存在电离平衡,因此1L 1mol?L-1的HAc溶液中含有氢离子数小于6.02×1023,故A错误;B、18g D2O(重水)物质的量=18g÷20g/mol=0.9mol。重水完全电解,则根据方程式2D2O→2D2+O2可知,转移的电子数约为0.9×2×6.02×1023,故B错误;C、二氧化氮和四氧化二氮间存在化学平衡2NO2 N2O4,标态下,22.4L NO2气体物质的量为1mol,所含氧原子数大于2×6.02×1023,小于4×6.02×1023,故C错误;D、乙烯和丙烯的最简式均是CH2,所以14g乙烯和丙烯的混合物中,含有共用电子对数目约为
N2O4,标态下,22.4L NO2气体物质的量为1mol,所含氧原子数大于2×6.02×1023,小于4×6.02×1023,故C错误;D、乙烯和丙烯的最简式均是CH2,所以14g乙烯和丙烯的混合物中,含有共用电子对数目约为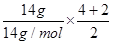 ×6.02×1023=3×6.02×1023,故D正确,答案选D。
×6.02×1023=3×6.02×1023,故D正确,答案选D。
本题难度:一般