ʱ��:2017-03-05 13:36:51
1��ѡ���� ��NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ�?��
A�����³�ѹ�£�17g��(��14CH3)������������Ϊ9NA
B��pH=1��ϡ�����к��е�H+ ��Ϊ0.1NA
C����״���£�0.1molCl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA
D�������£�20 L pH��12��Na2CO3��Һ�к��е�OH��������Ϊ0.2NA
�ο��𰸣�D
���������A�У���(��14CH3)��������AΪ17��������Z = 6+3��1 = 9����������N = A��Z = 8�����17g��(��14CH3)������������Ϊ8NA����ѡ�����B��û��ע��ϡ�����������ʲ��ܼ���H+ ����ֻ��д��c(H+ ) = 0.1mol/L����ѡ�����C��Cl2ֻ��������ˮ����ת�Ƶ�����С��0.1NA����ѡ�����D�У� pH��12��OH��Ũ��Ϊ0.01mol/L����20 L���е�OH��������Ϊ0.2NA����ѡ����ȷ��
�����������漰�˰���٤�������ļ��㣬��Ҫѧ�����ⷽ��Ĺ�ʽ�ͼ��㷽���������գ�ϸ�ڷ���ע��Է��ӣ�ԭ�ӣ����ӵĸ��������
�����Ѷȣ�һ��
2��ѡ���� ��NA�ǰ����ӵ���������ֵ������˵����ȷ����
A��0.1mol��L��1��NaCl��Һ�У�Na+����ĿΪ0.1NA
B��23 g �������ڳ��µĿ����г������������������ȫȼ��ת�Ƶ��ӵ���Ŀ��ΪNA
C��7.8g Na2O2�к��е�������������Ŀ��Ϊ0.1NA
D����״���£�22.4Lˮ�з��Ӹ���ΪNA
�ο��𰸣�B
���������A���Ȼ�����Һ�����δ֪���������ӵ���Ŀ�����㣬����B��23gNa�����ʵ�����1mol��������������Ӧ���������ƻ��ǹ������ƣ�Na��ȫ��Ӧת�Ƶ��ӵ����ʵ���ʼ����1mol��������Ŀ��NA����ȷ��C��7.8g�������Ƶ����ʵ�����0.1mol�����к��е��������������ӣ���������O22-���������������ӵ������ʵ�����0.3mol��������������ĿΪ0.3NA������D����״����ˮ�������壬����22.4Lˮ�����ʵ�������1mol���������Ŀ����NA������ѡB��
���㣺���鰢��٤�������������ļ����ϵ
�����Ѷȣ�һ��
3�������� �谢���ӵ�����ΪNA����
��1��2mol H2O�����ķ��Ӹ�����17g OH ���ӵ���Ŀ֮��Ϊ?��
���ӵ���Ŀ֮��Ϊ?��
��2��m��ˮ������Ϊn g����1��ˮ����ˮ���ӵĸ���Ϊ?��
�ο��𰸣���ÿ��4�֣���8�֣�2:1? nNA/18m
�����������1��17g OH ���ӵ����ʵ�����17g��17g/mol��1mol����˸���
���ӵ����ʵ�����17g��17g/mol��1mol����˸���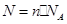 ��֪������������Ŀ֮����2�U1��
��֪������������Ŀ֮����2�U1��
��2��m��ˮ������Ϊn g����1��ˮ��������n/mg������1��ˮ�����ʵ�����n/mg��18g/mol��n/18m mol����˸���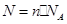 ��֪��1��ˮ����ˮ���ӵĸ���ΪnNA/18m
��֪��1��ˮ����ˮ���ӵĸ���ΪnNA/18m
�������ڽ������ʵ������йؼ���ʱ���ؼ�������Ӧ�ü�����ϵʽ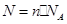 ��n��m/M��
��n��m/M��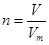 ��
��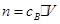 ��Ȼ������������ʽ���㼴�ɡ�
��Ȼ������������ʽ���㼴�ɡ�
�����Ѷȣ�һ��
4��ѡ���� ���й��ڡ�Ħ������˵������ȷ���� �� ��
A��Ħ����һ��������
B��Ħ����ʾ���ʵ���
C��Ħ�������ʵ����ĵ�λ
D��Ħ���DZ�ʾ���������ĵ�λ
�ο��𰸣�C
���������Ħ���ǹ��ʵ�λ�ƹ涨��7������������֮һ�������ʵ����ĵ�λ�����ѡ����C��
���㣺������ڡ�Ħ������˵����֪ʶ��
�����Ѷȣ�һ��
5��ѡ���� ����250mL0.10mol/L��������Һʱ������ʵ�������ʹ���Ƶ���ҺŨ��ƫ�ߵ��ǣ�������
A������ƿ����ˮ��δ�������ﴦ��
B������ʱ�����ӿ̶���
C������Ͳ��ȡŨ����ʱ����ˮϴ����Ͳ2��3�Σ�ϴ��Һ�����ձ���
D�����ݺ�ת����ƿ���Σ�����Һ����͵���ڿ̶��ߣ��ٲ��Ӽ���ˮ���̶���
�ο��𰸣�C
���������
�����Ѷȣ���