时间:2017-03-05 13:28:17
1、选择题 在核磁共振氢谱中出现两组峰,其氢原子数之比为3∶2的化合物是
[? ]
A.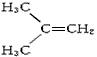
B.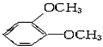
C.
D.
参考答案:D
本题解析:
本题难度:一般
2、选择题 在同温同压下,决定气体体积大小的因素是
A.气体的种类
B.分子间的平均距离
C.分子本身的大小
D.气体的分子数
参考答案:D
本题解析:分析:同温同压下,气体的分之间距离相等,影响气体体积的主要因素是气体的分子数.
解答:影响气体的体积的因素有:分子大小,数目以及分子之间的距离,同温同压下,气体的分之间距离相等,分子大小与分子之间的距离相比较可忽略,决定气体体积的主要因素是气体的分子数.
故选D.
点评:本题考查阿伏加德罗定律,题目难度较小,注意把握影响气体体积的因素,学习中注重相关基础知识的积累.
本题难度:困难
3、选择题 下列说法不正确的是
A.配一定物质的量浓度溶液实验中,容量瓶用蒸馏水洗净后即可使用,不需要干燥和润洗
B.“硝基苯制备”实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触
C.变色硅胶干燥剂含有CoCl2,干燥剂呈蓝色时,表示不具有吸水干燥功能
D.除去干燥CO2中混有的少量SO2,可将混合气体通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
参考答案:C
本题解析:分析:A、根据配一定物质的量浓度溶液实验中,容量瓶用蒸馏水洗净后不影响溶液的体积;
B、根据温度计的作用;
C、根据硅胶中加入的CoCl2是一种能指示吸水情况的干燥剂,它在未吸水时呈蓝色,吸足水后变粉红色.
D、根据除杂的条件来解答.
解答:A、因配一定物质的量浓度溶液实验中,容量瓶用蒸馏水洗净后不影响溶液的体积,浓度不变,所以不需要干燥和润洗,故A正确;
B、因温度计是测量水浴的温度,所以作水银球不能与烧杯底部和烧杯壁接触,故B正确;
C、因硅胶中加入的CoCl2是一种能指示吸水情况的干燥剂,它在未吸水时呈蓝色,吸足水后变粉红色,故C错误;
D、因酸性KMnO4溶液能氧化SO2,不与CO2反应,浓硫酸能吸收CO2中的水蒸气,故D正确;
故选C.
点评:本题主要考查了一些实验操作,难度不大,根据课本知识即可完成,选项C为学生解答中的难点.
本题难度:一般
4、填空题
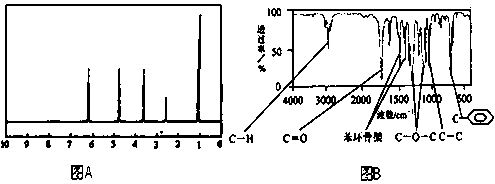
参考答案:(1)C9H10O2
(2)bc
(3)C6H5COOCH2CH3
(4)6
本题解析:
本题难度:一般
5、选择题 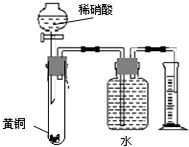 下列对有关实验的描述不正确的是
下列对有关实验的描述不正确的是
A.在浓氨水中加入生石灰可以制取少量的NH3
B.用水就可以一次性鉴别溴苯、苯、乙酸三种物质
C.用如右图所示的装置可以测定黄铜(Cu、Zn合金)中Zn的含量
D.除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是H2O、Ba(OH)2、Na2CO3、HCl
参考答案:C
本题解析:分析:A、生石灰可以吸收氨水中的水,让其中的氨气挥发出来;
B、溴苯和水互不相溶,且密度比水大,苯和水互不相溶,密度比水小,乙酸和水互溶;
C、Cu、Zn均能和稀硝酸反应生成对应的盐和一氧化氮,用排水量气法时,洗气瓶的导管要短进长出;
D、粗盐的提纯步骤:先溶解粗盐,再过滤,然后向滤液中加入氢氧化钡,除去粗盐中的硫酸根离子和镁离子,再过滤,向滤液中加入碳酸钠,除去粗盐中的钙离子和多余的钡离子,最后加盐酸,除去多余的碳酸根离子;
解答:A、生石灰可以吸收氨水中的水,让其中的氨气挥发出来,可以在浓氨水中加入生石灰可以制取少量的NH3,故A正确;
B、溴苯和水互不相溶,且密度比水大,混合后分层,上层是水,下层是溴苯,苯和水互不相溶,密度比水小,混合后分层,上层是苯,下层是水,乙酸和水互溶,不分层,故B正确;
C、Cu、Zn均能和稀硝酸反应生成对应的盐和一氧化氮,但是用排水量气法时,洗气瓶的导管要短进长出,故C错误;
D、粗盐的提纯步骤:先溶解粗盐,再过滤,然后向滤液中加入氢氧化钡,除去粗盐中的硫酸根离子和镁离子、铁离子等,再过滤,向滤液中加入碳酸钠,除去粗盐中的钙离子和多余的钡离子,最后加盐酸,除去多余的碳酸根离子,碳酸钠必须加在氢氧化钡的后面,最后加盐酸,故D正确;
故选C.
点评:本题考查学生对有关化学实验基本知识的掌握程度,要求学生熟记所学知识,学以致用.
本题难度:困难