时间:2017-03-05 13:27:18
1、选择题 下列有关电子云和原子轨道的说法正确的是
A.原子核外的电子象云雾一样笼罩在原子核周围,故称电子云
B.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
C.p能级的原子轨道呈纺锤形,随着电子层的增加,p能级原子轨道也在增多
D.与s原子轨道的电子相同,p原子轨道电子的平均能量随能层的增大而增加
参考答案:D
本题解析:试题分析:电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述,电子云实际上不存在的,A不正确;B不正确,电子在核外电子空间的运动状态是不固定的;p能级原子轨道只有3个,C不正确,所以正确的答案选D。
考点:考查电子云和原子轨道的有关正误判断
点评:该题是常识性知识的考查,试题贴近教材,基础性强,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于激发学生的学习兴趣和学习积极性。
本题难度:困难
2、选择题 在下列比较中,正确的是
A.热稳定性:PH3>H2S>HCl>HF
B.分子中的键角:CH4=H2O<CO2
C.分子间作用力:HF>HCl>HBr>HI
D.晶体熔点:石英>食盐>冰>干冰
参考答案:D
本题解析:
本题难度:困难
3、选择题 下列各组元素性质递变情况错误的是
A.Li、Be、B原子最外层电子数依次增多
B.N、O、F、Ne电子层数依次增多
C.P、S、Cl元素最高正化合价依次升高
D.O、S、Se氧化性依次减弱
参考答案:B
本题解析:
本题难度:困难
4、简答题 下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
| a | f y h i b | e j c d d g l | |||||||||||||||||||||||||||||||||||
参考答案:(1)由元素在周期表中的位置可知,d为Fe元素,原子序数为26,则Fe3+的核外电子排布式的1s222s2p63s23p63d5,故答案为:1s222s2p63s23p63d5;?
(2)e为Al元素,原子序数为13,其电子轨道表示式为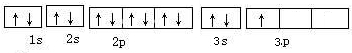
,
故答案为:
;
(3)y为N,a为H,则ya3分子为NH3,其电子式为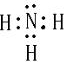
,空间构型为三角锥形,故答案为: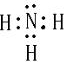
;三角锥形;
(4)b为Mg,e为Al,金属性Mg>Al,镁原子最外层为全满,失去1个电子较难,则第一电离能大,故答案为:Mg;Mg;?
(5)h为O,i为F,f为C,OF2分子中O原子上有2对孤电子对,σ键数为2,则杂化类型sp3,CO32-中无孤电子对,σ键数为3,则杂化类型sp2,则空间构型为平面正三角形,
故答案为:sp3;平面正三角形.
本题解析:
本题难度:一般
5、选择题 既能与H2S反应,又能与溴水反应的是(?)
⑴? Na2S溶液? ⑵? SO 2溶液?⑶ CuSO4溶液?(4)FeCl2溶液
2溶液?⑶ CuSO4溶液?(4)FeCl2溶液
A? ⑴⑵⑶⑷?B ⑴ ⑵? C? ⑵⑶⑷(5)?D ⑵⑷
参考答案:B
本题解析:略
本题难度:一般