ʱ��:2017-03-05 13:19:40
1�������� ��6�֣�����ʯ��18.5g�������40g��ϼ��ȣ��ټ�������������ڱ���µ�������ڽ�������������100mL ˮ�У��õ��ܶ�Ϊ0.868 g/cm3 �İ�ˮ���������ð�ˮ�����ʵ���Ũ�ȡ�
�ο��𰸣�11.2L ��4mol/L
�����������
�����Ѷȣ���
2��ѡ���� ����ȷ�������Ȼ��ƹ�������0.1mol/L���Ȼ�����Һ500mL����Ҫ�õ��������ǣ�������
����ƿ���ձ���1000mL������ƿ��500mL������ƿ�ݽ�ͷ�ιܢ�������
A���ڢܢݢ�
B���ڢۢݢ�
C���٢ڢܢ�
D���ڢܢ�
�ο��𰸣����Ѿ���������Ȼ�������0.1mol/L���Ȼ�����Һ500mL���漰�IJ����У��ܽ��Ȼ��ƣ��õ��ձ��Ͳ�������ת����Һ���õ���������500mL����ƿ��ϴ���ձ��Ͳ�������������Һ���õ���ͷ�ιܣ�����ʹ�õ������У��ձ�����������500mL����ƿ����ͷ�ιܣ����ڢܢݢޣ�
��ѡA��
���������
�����Ѷȣ���
3������� ij������ܶ�Ϊ1.095g?cm-3����������Ϊ10.0%���Լ��㣺
��1������������ʵ���Ũ���Ƕ��٣�
��2��200mL�������������п����ַ�Ӧ������������������״���£��Ƕ���L��
�ο��𰸣���1���ܶ�Ϊ1.095g?cm-3����������Ϊ10.0%����������ʵ���Ũ��c=1000��1.095��10%36.5mol/L=3mol/L��
�𣺸���������ʵ���Ũ��Ϊ3mol/L��
��2��200mL��������n��HCl��=0.2L��3mol/L=0.6��Դ:91������ 91EXAm.orgmol���ɷ���ʽZn+2HCl=ZnCl2+H2����֪�����ɵ����������ʵ���Ϊ��0.6mol��12=0.3mol���������������Ϊ��0.3mol��22.4L/mol=6.72L��
�𣺱�״�����������������Ϊ6.72L��
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵������ȷ����
? [? ]
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ����֪C6H5ONa��CO2��H2O�D��C6H5OH��NaHCO3��ij�л���Ľṹ��ʽ���£�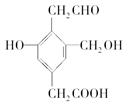
Na��NaOH��NaHCO3�ֱ�������ʵ����ĸ�����ǡ�÷�Ӧʱ��Na��NaOH��NaHCO 3�����ʵ���֮��Ϊ
A��3��3��2
B��3��2��1
C��1��1��1
D��3��2��2
�ο��𰸣�B
������������Ʒ�Ӧ���д��ǻ������ǻ����Ȼ������������Ʒ�Ӧ�з��ǻ����Ȼ�����̼�����Ʒ�Ӧ��ֻ���Ȼ�������3��2��1
�����Ѷȣ���