时间:2017-03-03 01:10:57
1、实验题 Ba(NO3)2可用于生产绿色烟花、绿色信号弹、炸药等。某生产BaCO3、BaSO4的化工厂生产中排出大量的钡泥[主要含有BaCO3、BaSO3、Ba(FeO2)2等],该厂利用钡泥制取Ba(NO3)2晶体(不含结晶水),其部分工艺流程如下:
已知: ①Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7;
②Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9。?
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式说明提纯原理:?。
(2)酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为?。
(3)该厂结合本厂实际,选用的X为?(填序号),中和I使溶液中的?(填离子符号)的浓度减小。
A.BaCl2
B.Ba(OH)2
C.Ba(NO3)2
D.BaCO3
(4)最后的废渣中除原有的难溶性杂质外还含有?(填化学式)。
(5)测定所得Ba(NO3)2晶体的纯度:准确称取m1g晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m2g,则该晶体纯度的计算表达式为?。(已知Ba(NO3)2、BaSO4的式量分别为261、233)
参考答案:(16分)
(1)BaSO4(s)+CO32- BaCO3(s)+SO42-(3分)
BaCO3(s)+SO42-(3分)
(2)Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O(3分)
(3)D(2分)? Fe3+、H+(2分)
(4)BaSO4、Fe(OH)3(3分)
(5) ×100%(3分)
×100%(3分)
本题解析:(1)根据已知信息可知,5.1×10-9约为1.1×10-10的46倍,虽然Ksp(BaCO3)> Ksp(BaSO4),因此BaSO4可以转化为BaCO3,前提是增大碳酸根离子的浓度,使碳酸根离子与钡离子结合生成碳酸钡沉淀,导致BaSO4 (s) Ba2++SO42-的平衡向右移动,总反应为BaSO4(s)+CO32-
Ba2++SO42-的平衡向右移动,总反应为BaSO4(s)+CO32- BaCO3(s)+SO42-;
BaCO3(s)+SO42-;
(2)依题意推断,酸溶时Ba(FeO2)2与HNO3反应生成的两种硝酸盐分别是硝酸钡、硝酸铁,不涉及氧化还原反应,利用观察法可以配平该复分解反应方程式,即Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;
(3)氯化钡不能与氢离子反应,不能调节pH,且引入氯离子,故A选项错误;氢氧化钡与氢离子能反应,可以调节溶液pH,但是氢氧化钡是强碱,成本高,且容易导致溶液pH升高过快,超出中和I要求的pH范围,故B选项错误;硝酸钡不能与氢离子反应,故C选项错误;碳酸钡与氢离子能反应,生成钡离子、二氧化碳气体和水,既能调节溶液pH在4~5之间,又不引入新的杂质,故D选项正确;根据已知信息推导,硝酸是氧化性酸,钡泥酸浸之后溶液中无亚铁离子,加入碳酸钡溶液pH在4~5之间,既能减小氢离子溶液,又能促进铁离子完全水解,导致铁离子完全变为氢氧化铁沉淀,则中和I使溶液中的氢离子和铁离子的浓度减小;
(4)由于硝酸是强酸、强氧化性酸,则BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O、3BaSO3+2HNO3=3BaSO4+2NO↑+H2O,Ba(OH)2+2HNO3= Ba(NO3)2+2H2O,则最后的废渣中除原有的难溶性杂质外,还含有BaSO4、Fe(OH)3;(5)由于硫酸钡的式量为233,n=m/M,则硫酸钡的物质的量为m2/233 mol;由于反应Ba(NO3)2+H2SO4= BaSO4↓+2HNO3中Ba(NO3)2与BaSO4的系数之比等于物质的量之比,则晶体中Ba(NO3)2的物质的量为m2/233 mol;由于硝酸钡的式量为261,m=n?M,则晶体中硝酸钡的质量为261 m2/233g;由于晶体的质量为m1g,则晶体中硝酸钡的纯度计算表达式为261m2/233m1×100%。
本题难度:困难
2、选择题  一元弱酸HA(aq)中存在下列电离平衡:HA
一元弱酸HA(aq)中存在下列电离平衡:HA H++A-,如图将1.0 mol HA分子加入1.0 L水中,溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是
H++A-,如图将1.0 mol HA分子加入1.0 L水中,溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是
参考答案:C
本题解析:略
本题难度:简单
3、选择题 下列化学实验能达到目的是( )
A.用激光笔检验某KI溶液中是否溶有淀粉
B.加入适量溴水后过滤,可除去苯中的少量苯酚
C.向碘水中加入苯或酒精,均可从碘水中萃取碘
D.向AgCl沉淀中滴加少量KI溶液,可说明Ksp(AgCl)<Ksp?(AgI)
参考答案:A.KI溶液中溶有的淀粉是胶体,胶体有丁达尔现象,用激光笔检验,看到一条光亮的通路,说明含有淀粉,如不能说明没有淀粉,因碘化钾溶液没有丁达尔现象,故A正确;
B.溴易溶于苯,溴水与苯发生萃取,苯酚与溴水发生取代反应生成三溴苯酚,用溴水除杂,生成的三溴苯酚和过量的溴都能溶于苯,不能得到纯净的苯,并引入新的杂质,不能用来除杂,除去苯中的少量苯酚,应向混合物中加入NaOH溶液后分液,故B错误;
C.苯和水不互溶,且碘在苯中的溶解度大于在水中的溶解度,苯和碘不反应,所以苯能作萃取剂萃取碘水中的碘;酒精和水互溶,所以酒精不能作萃取剂,故C错误;
D.在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成,说明AgI难溶,AgCl比AgI的溶度积常数大,故D错误;
故选A.
本题解析:
本题难度:简单
4、选择题 难溶电解质AB2的饱和溶液中,[A2+]=xmol/L,[B-]=ymol/L,则Ksp值为( )
A.xy2
B.xy
C.xy2
D.4xy2
参考答案:难溶电解质AB2的电离方程式为AB2(s)?A 2+(aq)+2 B-(aq),
AB2饱和溶液中,c(A2+)=xmol?L-1,c(B-)=ymol?L-1,
则Ksp=c(A 2+).c2( B-)=xy2,
故选C.
本题解析:
本题难度:简单
5、填空题 (8分)25℃时,1L 0.01mol/LHCl溶液,水的离子积常数Kw为?,溶液中H+的物质的量浓度为?,水电离出的H+的物质的量浓度为?,向上述溶液中加入1L 0.008mol/L的NaOH溶液,反应后溶液的pH为??。
参考答案:(每空2分,共8分)1×10-14,0.01mol/L,1×10-12 mol/L,3
本题解析:常温下水的离子积常熟是1×10-14,盐酸是强酸,所以溶液中氢离子浓度是0.01mol/L,则溶液中OH-的浓度是1×10-12 mol/L,所以由水电离出的氢离子浓度也是1×10-12 mol/L。反应后溶液中的氢离子浓度是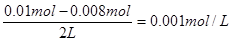 ,所以pH=3。
,所以pH=3。
本题难度:一般