时间:2017-03-03 01:06:43
1、简答题 实验室用NaCl固体配制1mol/L的NaCl溶液500mL,回答下列问题:
(1)请写出该实验的实验步骤:①计算,②称量,③______,④冷却,⑤______,⑥洗涤,⑦定容,⑧摇匀.用托盘天平称量样品时,若指针偏向右边,则表示______(填“左盘”或“右盘”)重.
(2)所需主要仪器为:托盘天平、药匙、500mL容量瓶、胶头滴管、______.
(3)从配制好的溶液中取出50mL,其中NaCl的物质的量浓度为______.
参考答案:(1)配制1mol/L的NaCl溶液500mL的步骤为:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等;使用托盘天平时,药品放在左盘,砝码放在右盘,若指针偏向右边,说明右边的砝码较重,
故答案为:溶解;移液(转移);右盘;
(2)配制500mL 1mol/L的NaCl溶液使用的仪器为:托盘天平、药匙、500mL容量瓶、胶头滴管、烧杯、玻璃棒,还缺少烧杯和玻璃棒;
故答案为:烧杯、玻璃棒;
(3)配制好的溶液中取出50mL,由于溶液是均一的,所以NaCl的物质的量浓度还是1mol/L,
故答案为:1mol/L.
本题解析:
本题难度:一般
2、实验题 用Na2CO3・10H2O晶体,配制0.2 mol/L的Na2CO3溶液480 mL。
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少_____________,____________;
(2)应用托盘天平称取Na2CO3・10H2O的晶体的质量为_________________g;
(3)配制溶液时有以下几个操作: ①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容正确的操作顺序是__________________(填序号)。
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空。
①碳酸钠失去了部分结晶水
②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有____________,无影响的有________。(填序号)
参考答案:(1)500 mL容量瓶;胶头滴管
(2)28.6 g
(3)⑤①④⑥③⑦②
(4)①④
本题解析:
本题难度:一般
3、选择题 在下列条件下,两种气体的分子数一定相等的是 ( )。
A.同密度、同压强的N2和C2H4
B.同温度、同体积的O2和N2
C.同体积、同密度的C2H4和CO
D.同压强、同体积的O2和N2
参考答案:C
本题解析:根据阿伏加德罗定律及其推论可以判断A、B、D错误。C项,同体积、同密度的C2H4和CO质量相等,C2H4和CO的相对分子质量都是28,所以,等质量时两者物质的量相等,分子数也相等。
本题难度:一般
4、选择题 25℃时,某物质(无结晶水)溶解度为Sg,其摩尔质量为M g/mol,饱和溶液密度为dg/cm3。则其饱和溶液的物质的量浓度为
A.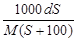 mol/L
mol/L
B.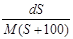 mol/L
mol/L
C.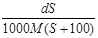 mol/L
mol/L
D.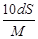 mol/L
mol/L
参考答案:A
本题解析:溶解度为S,则饱和溶液的质量分数是S/(S+100)。又因为物质的量浓度= ,所以选项A正确,答案选A。
,所以选项A正确,答案选A。
本题难度:一般
5、选择题 同温同压下,相同体积的H2和CO2气体,具有相同的 ( )
A.质量
B.原子数
C.分子数
D.摩尔质量
参考答案:C
本题解析:同温同压下,相同体积的H2和CO2气体,具有相同的物质的量,相同的分子数。答案选C。
考点:阿伏伽德罗定律
点评:同温同压下,具有相同体积的任何气体具有相同的分子数。
本题难度:一般