时间:2017-03-03 00:57:33
1、选择题 有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg ,室温下实验室用0.01 mol・L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如图所示。下列有关叙述正确的是
,室温下实验室用0.01 mol・L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如图所示。下列有关叙述正确的是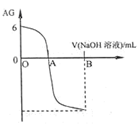
A.A点时加入氢氧化钠溶液体积为20 mL
B.室温时0.01 mol・L-1的醋酸溶液pH=6
C.OA段溶液中:c(CH3COO-)> c(CH3COOH)
D.若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH) = c(OH-) - c(H+)
2、选择题 下列有关说法正确的是
A.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差
B.常温下,MgO(s)+C(s)=Mg(s)+CO(g)不能自发进行,则其△H>0
C.在NaCl和KBr的混合溶液中滴加AgNO3溶液,一定先产生淡黄色沉淀
D.加热0.1 mol・L-1Al2(SO4)3溶液,水解程度增大、溶液的酸性增强
3、选择题 下列现象不能用盐类水解知识解释的是
A.明矾能用于净水
B.泡沫灭火器的原理
C.铜绿的生成
D.配置FeCl2溶液时加入少量的盐酸
4、填空题 (16分)Na2CO3俗称纯碱、苏打,NaHCO3俗称小苏打,两者在日常生活和工业生产中都有着广泛的应用。某化学兴趣小组设计了如下实验来探究两者的某些性质。请你根据所学知识帮他们完成有关的设计和实验。
(1)甲同学测定两者的酸碱性:各取一定量的固体溶于水,配成相同浓度的溶液,测定其pH值,测定结果为Na2CO3、NaHCO3的pH分别为a和b(a、b均大于7),则a b(填“大于”“等于”或“小于”),测定溶液的pH值所用的主要仪器有:pH试纸、表面皿、 和标准比色卡。
(2)有关①100mL0.1 mol・L-1NaHCO3、 ②100mL0.1 mol・L-1Na2CO3,两种溶液的叙述不正确是
A.NaHCO3溶液中:c (H+)+c (Na+)=" c" (HCO3-)+2c(CO32-)+c(OH-)
B.Na2CO3溶液中:2c (Na+)=" c" (HCO3-)+c(CO32-)+c(H2CO3)
C.①溶液中:c(CO32-)>c(H2CO3)
D.②溶液中:c(HCO3-)>c(H2CO3)
(3)乙同学取一定量的碳酸钠溶液于试管中,滴加2~3滴酚酞试液,发现溶液变红,继续滴加BaCl2溶液,预计可观察到 ,请你结合必要的离子方程式,应用平衡的观点解释有关现象的产生: 。
(4)丙同学往10mL0.10 mol・L-1的Na2CO3溶液中逐滴滴加0.10 mol・L-1的HCl,当溶液中的:
c(Na+)=c(Cl-)+c(HCO3-)+2c(CO32-),此时溶液呈 (填“酸性”、“中性”或“碱性”),所用HCl的体积 10mL。(填“大于”“等于”或“小于”)
(5)已知:Ksp(CaCO3)=4.96×10-9,不考虑其它因素影响,现将0.40 mol・L-1的Na2CO3溶液和0.20 mol・L-1的CaCl2溶液等体积混合,则混合后溶液中Ca2+浓度为 mol・L-1。
5、填空题 (14分)A、B、C、D为原子序数依次增大的四种第三周期元素,其单质及其化合物的性质或结构信息如下表所述。
| 元素 | A | B | C | D |
| 性质 结构 信息 | 工业上常用电解熔融AD2制取A的单质。 | B的最外层电子数比最内层电子数多1。 | C的最高价氧化物的水化物经聚合、脱水,可作袋装食品干燥剂。 | D的一种气态氧化物甲对空气的相对密度为3,它溶于水得到单一溶质的弱酸性溶液(有漂白性),该溶液光照后酸性增强。 |