时间:2017-03-03 00:50:02
1、选择题 体积相同浓度均为0.1mol?L-1的NaOH溶液、氨水,分别稀释m倍、n倍,溶液的pH都变成9,则m和n的关系正确的是( )
A.m>n
B.m=n
C.m<n
D.不能确定
参考答案:氢氧化钠是强电解质完全电离,一水合氨是弱电解质,在水溶液里部分电离,相同浓度的两种溶液中,氢氧化钠溶液的pH大于氨水,加水稀释促进一水合氨电离,但一水合氨仍然存在电离平衡,电离程度仍然小于氢氧化钠,所以要使稀释后溶液的PH相等,则氢氧化钠需要稀释倍数大于氨水,
故选A.
本题解析:
本题难度:一般
2、选择题 某化学研究性学习小组对电解质溶液作如下的归纳总结(均在常温下),其中正确的是?
① pH=1的强酸溶液,加水稀释后,溶液中各离子浓度都会降低
② 1 L 0.50 mol・L-1NH4Cl 溶液与2 L 0.25 mol・L-1NH4Cl 溶液含NH4+ 物质的量完全相等
③ pH相等的四种溶液:a.CH3COONa? b.C6H5ONa? c.NaHCO3?d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d < b < c < a
④ pH=8.3的NaHCO3溶液:c(Na+) > c(HCO3-) > c(CO32-)> c(H2CO3)
⑤ pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-) ≤ c(H+)
⑥pH=4、浓度均为0.1mol・L-1的CH3COOH、CH3COONa混合溶液中:c(CH3COO-)+c(OH-) > c(CH3COOH)+c(H+)
A.①②④
B.①③⑤
C.③⑤⑥
D.②④⑥
参考答案:C
本题解析:① pH=1的强酸溶液,加水稀释后,溶液中各离子浓度都会降低,但是氢氧根离子浓度会升高,错误;② 1 L 0.50 mol・L-1NH4Cl 溶液与2 L 0.25 mol・L-1NH4Cl 溶液含NH4+ 物质的量完全相等,这个说法也是错误的,原因是两种溶液中氯化铵的浓度不一样大,水解程度不一样。③ pH相等的四种溶液:a.CH3COONa? b.C6H5ONa? c.NaHCO3?d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d < b < c < a,正确。因为酸性强弱顺序为:醋酸、碳酸、苯酚,所以相应的钠盐的碱性强弱就为苯酚钠、碳酸氢钠、醋酸钠,四种溶液的溶质的物质的量浓度由小到大的顺序为:d < b < c < a;④ pH=8.3的NaHCO3溶液中,碳酸氢根离子存在水解和电离子两种趋势,又由于溶液显碱性,因此水解程度大于电离程度,所以有:c(Na+) > c(HCO3-)> c(H2CO3) > c(CO32-),所以错误;⑤ pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-) ≤ c(H+),正确;⑥pH=4、浓度均为0.1mol・L-1的CH3COOH、CH3COONa混合溶液中,表明溶液显酸性,也就是说醋酸的电离程度比醋酸根离子的水解程度大。所以有: c(CH3COOH)<c(Na+),再根椐电荷守恒:c(CH3COO-)+c(OH-) = c(Na+)+c(H+),于是就有以下关系式:c(CH3COO-)+c(OH-) > c(CH3COOH)+c(H+)。因此选C。
本题难度:一般
3、填空题 已知金属离子从开始形成氢氧化物沉淀到沉淀完全时溶液的pH。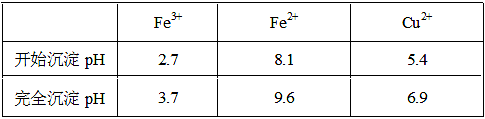
(1)实验室配制FeCl2溶液时需加入少许盐酸和铁粉,若只加盐酸、不加铁粉,溶液中会发生什么变化,用离子方程式表示为:?;
(2)氯化铜晶体(CuCl2・2H2O)中含FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下面所示的操作步骤进行提纯。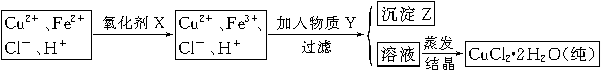
①加氧化剂X的目的是?,下列氧化剂中最适合作氧化剂X的是?(填序号);
A.NaClO
B.H2O2
C.KMnO4
D.HNO3
②物质Y的化学式是?;加入物质Y的目的是调节溶液的pH至a,使Fe3+沉淀完全,则a的范围是?;若25℃时,a=3的溶液中,c(Fe3+)=?mol・L-1。(25℃时,Ksp[Fe(OH)3]=4.0×10-38)
(3)欲将CuCl2・2H2O加热制得无水CuCl2,将采用什么方法和措施?__________。
参考答案:(1)4Fe2++O2+4H+ 4Fe3++2H2O
4Fe3++2H2O
(2)①将Fe2+氧化为Fe3+?B?②CuO[或Cu(OH)2或CuCO3] 3.7≤a<5.4? 4.0×10-5
(3)在HCl气氛下蒸发,以抑制CuCl2水解
本题解析:(1)实验室配制FeCl2溶液时需加入少许盐酸和铁粉,目的是为了防止亚铁离子被氧化和析出沉淀,若只加盐酸、不加铁粉,溶液的亚铁离子被氧化为铁离子,其离子方程式为:4Fe2++O2+4H+ 4Fe3++2H2O;(2)氯化铜晶体(CuCl2・2H2O)中含FeCl2杂质,加氧化剂X的目的是将Fe2+氧化为Fe3+,最适合作氧化剂X的是H2O2,因为其氧化产物无污染,且容易除去;②物质Y是为了调节溶液的pH,并且不能引入新的杂质,或者是杂质很容易就除去了,故Y应该为CuO[或Cu(OH)2或CuCO3],右表可以看出,铁离子在pH为3.7时沉淀完全,而铜离子在5.4时才开始沉淀,故a的范围为3.7≤a<5.4;若25℃时,a=3的溶液中,则c (OH-)=10-11mol/L,c(Fe3+)=4.0×10-38/(10-11)3mol/L= 4.0×10-5 mol/L;(3)欲将CuCl2・2H2O加热制得无水CuCl2,因为其为强酸弱碱盐,所以必须在HCl气氛下蒸发,以抑制CuCl2水解。
4Fe3++2H2O;(2)氯化铜晶体(CuCl2・2H2O)中含FeCl2杂质,加氧化剂X的目的是将Fe2+氧化为Fe3+,最适合作氧化剂X的是H2O2,因为其氧化产物无污染,且容易除去;②物质Y是为了调节溶液的pH,并且不能引入新的杂质,或者是杂质很容易就除去了,故Y应该为CuO[或Cu(OH)2或CuCO3],右表可以看出,铁离子在pH为3.7时沉淀完全,而铜离子在5.4时才开始沉淀,故a的范围为3.7≤a<5.4;若25℃时,a=3的溶液中,则c (OH-)=10-11mol/L,c(Fe3+)=4.0×10-38/(10-11)3mol/L= 4.0×10-5 mol/L;(3)欲将CuCl2・2H2O加热制得无水CuCl2,因为其为强酸弱碱盐,所以必须在HCl气氛下蒸发,以抑制CuCl2水解。
点评:本题考查了盐类水解,溶度积等知识点,这些考点都是高考考查的重点和难点,本题有一定的综合性,关键是要根据表中的数据进行解答,本题难度中等。
本题难度:一般
4、选择题 有常温下物质的量浓度均为0.1 mol/L的①氨水②NH4Cl溶液③Na2CO3溶液?④NaHCO3溶液,下列说法正确的是(?)
A.4种溶液pH的大小顺序:①>④>③>②
B.等体积的①和②溶液混合后若pH>7:c(Cl-)>c(N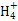 )
)
C.溶液①、③由水电离产生的c(OH-):①<③
D.溶液③、④等体积混合后,溶液中c(C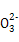 )>c(HC
)>c(HC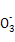 )
)
参考答案:C
本题解析:Na2CO3水解程度大于NaHCO3,碱性强,故4种溶液pH的大小顺序:①>③>④>②,A错;根据溶液电中性:c(N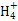 )+c(H+)=c(Cl-)+c(OH-),由溶液的pH>7,可知c(H+)<c(OH-),故c(N
)+c(H+)=c(Cl-)+c(OH-),由溶液的pH>7,可知c(H+)<c(OH-),故c(N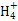 )>c(Cl-),B错;Na2CO3水解促进水的电离,NH3・H2O电离抑制水的电离,故水电离产生的c(OH-):①<③,C对;③、④等体积混合后以C
)>c(Cl-),B错;Na2CO3水解促进水的电离,NH3・H2O电离抑制水的电离,故水电离产生的c(OH-):①<③,C对;③、④等体积混合后以C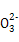 的水解为主,且C
的水解为主,且C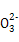 水解生成HC
水解生成HC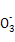 ,故溶液③、④等体积混合后,溶液中c(C
,故溶液③、④等体积混合后,溶液中c(C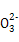 )<c(HC
)<c(HC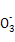 ),D错。
),D错。
本题难度:一般
5、选择题 已知同温同浓度时,①H2CO3比H2S的电离(“-”级电离)常数大,②H2S比HCO3-的电离常数大(即H2S的K1比H2CO3的K2大),根据酸与盐的反应规律,下列反应中不正确的是
[? ]
A.Na2CO3+H2S=NaHCO3+NaHS
B.Na2S+H2O+CO2=NaHS+NaHCO3
C.2NaHCO3+H2S=Na2S+2H2O+2CO2
D.NaHS+H2O+CO2=NaHCO3+H2S
参考答案:C
本题解析:
本题难度:一般