时间:2017-03-03 00:46:44
1、推断题 下图是物质A-K的相互转变关系图。已知A是由原子个数比为1:2:4的三种常见元素组成的化合物,在隔绝空气下A加热分解得到等物质的量的B、C、D三种氧化物;常温下B、C、F是无色气体,J为黄绿色气体,G、H为常见金属单质,部分反应条件未注明。 
请回答:
(1)A的化学式___________。
(2)H元素在元素周期表中的位置_____________
(3)写出C与E反应的化学方程式并注明条件_________________
(4)写出反应②的化学方程式__________________。
(5)反应③可在溶液中进行,其离子方程式为_________________
(6)请列举两例说明D+G反应原理在生产中的应用: ①_____________②_______________。
参考答案:(l)FeC2O4
(2)第四周期Ⅷ族
(3)CO+H2O(g)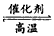 CO2+ H2
CO2+ H2
(4) FeO+ CO Fe + CO2
Fe + CO2
(5)2Fe3++3ClO- +10OH-=2FeO42-+3Cl- +5H2O
(6)①焊接钢轨;②冶炼高熔点金属(钒、铬、锰等)
本题解析:
本题难度:一般
2、填空题 如图转化关系中A-H为中学常见化合物,甲、乙、丙、丁为常见单质,其中甲、丁常温为气体.已知单质乙、化合物A为黄色(或淡黄色)固体.乙经过连续与甲反应后,再与水化合,是工业上制H的反应过程.B、F两种气体都能使澄清石灰水变浑浊.(部分反应物或产物略去)
(1)写出下列反应的化学方程式:
A与B______,甲与F______
(2)工业制H时,甲与F反应发生在______(设备名称)
(3)写出丙与D溶液反应的离子方程式______
(4)常温时H的浓溶液与丙物质并不能看到明显的反应现象,原因是______.
参考答案:本题关键是从化合物A是淡黄色固体、单质乙是黄色固体,推断出A为Na2O2,乙为S,判断甲为O2,D为NaOH,F为二氧化硫SO2,G为SO3,H为H2SO4;B、F两种气体都能使澄清石灰水变浑浊,所以推断出B为二氧化碳CO2;E为Na2CO3;丙单质和氢氧化钠反应,也可以和硫酸反应,说明单质为铝;综合分析判断,结合反应,写出个步反应为:
A(Na2O2)+H2O→甲(O2)+D(NaOH);A(Na2O2)+B(CO2)→甲(O2)+E(Na2CO3);甲(O2)+乙(S)→F(SO2)→G(SO3)→H(H2SO4);D(NaOH)+丙(Al)→丁(NaAlO2),H(H2SO4)+丙(Al)→丁(NaAlO2),;所以拍得出的物质分别为:A、Na2O2;B、CO2;D、NaOH;E、Na2CO3;F、SO2;G、SO3;H、H2SO4;甲、O2;乙、S;丙、Al;
(1)A与B发生反应生成碳酸钠和氧气,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;甲与F发生反应生成三氧化硫,化学方程式为:2SO2+O2催化剂.△2SO3
故答案为:2Na2O2+2CO2=2Na2CO3+O2;2SO2+O2催化剂.△2SO3
(2)工业制硫酸时,二氧化硫的催化氧化反应在接触室内完成反应,所以设备名称为接触室,故答案为:接触室;
(3)丙与D溶液反应是金属铝和氢氧化钠反应生成偏铝酸钠和氢气,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)常温下金属铝在浓硫酸中 发生钝化现象,不再继续反应,故答案为:铝在浓硫酸中表面形成致密的氧化膜,阻止内部金属的反应(或铝在浓硫酸中发生钝化);
本题解析:
本题难度:一般
3、选择题 A、B、C、D、E均含有同一种短周期元素,其中A是单质,B常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物.下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 物质编号 | 物质转化关系 | A | D | E ① | 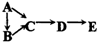 Si SiO2 H2SiO3 ② N2 NO2 HNO3 ③ S SO3 H2SO4 ④ Na Na2O2 NaOH |
参考答案:①Si的氧化物只有二氧化硅,二氧化硅不溶于水,不与水反应,不能一步得到硅酸,故①错误;
②若A为氮气,与氢气化合生成氨气,与氧气反应生成NO,NO与氧气反应生成二氧化氮,二氧化氮与水反应生成硝酸,符合题意,故②正确;
③若A是S单质,与氢气化合生成硫化氢,与氧气反应生成二氧化硫,二氧化硫再与氧气反应生成三氧化硫,三氧化硫与水化合生成硫酸,符合题意,故③正确;
④若A是钠,则B为氢化钠,为固态,且NaH不能反应生成氧化钠,不符合题意,故④错误;
故选A.
本题解析:
本题难度:简单
4、实验题 (9分)X、Y和W为原子序数依次递增的短周期主族元素,X和Y同主族,且能形成气态化合物YX2。试回答下列问题:
(1)W的原子序数为?。
(2)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成、再向该试管中加入?(填字母),可以看到白色沉淀生成。
A.氨水? B.稀盐酸? C.硝酸钠? D.氯化钙溶液
(3)某小组设计如图所示的装置图(图中夹持和加热装置略去),研究W2的性质。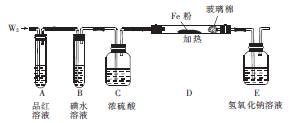
①装置A、D中观察到的现象分别为?、?。
②若装置B中装有5.0 mL l.0×10-3 mol·L-1碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为?。
(4)若由元素Y和X组成-2价酸根离子M,M中Y和X的质量比为4:3,已知1mol W2与含1mol M的溶液能恰好完全反应,反应时仅观察到有浅黄色沉淀产生。取反应后的上层清液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。则W2与含M的溶液反应的离子方程式为?。
参考答案:
本题解析:略
本题难度:一般
5、填空题 下图转化关系中,A、B、C、D、E都是短周期元素的单质,在常温常压下A是固体,其余都是气体,且C呈黄绿色。化合物H和I两种气体相遇时产生白烟。化合物G的焰色反应为黄色。反应①和②均在溶液中进行。
请按要求回答下列问题。
(1)写出下列物质的化学式D?、F?
(2)反应①的离子方程式为?。
(3)向K溶液中加入硝酸酸化的硝酸银溶液,反应的现象为?。
(4)将少量单质C通入盛有淀粉KI溶液的试管中,液体变为蓝色。该反应的离子方程式为?。这说明单质C的氧化性?于单质碘(填“强”或“弱”)。
参考答案: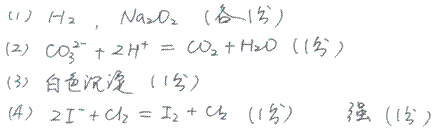
本题解析:略
本题难度:简单