ʱ��:2017-03-03 00:41:11
1��ѡ���� ������Ԫ��X��Y��Z��ԭ����������������ԭ�ӵ�����������֮��Ϊ13��X��Y��Zλ���������ڣ�Zԭ��������������Xԭ���ڲ��������3������Yԭ��������������3��������˵����ȷ����
[? ]
A.X������������Ӧ��ˮ������������
B.Y�������������ӻ�����
C.X���⻯���ˮ��Һ�ڿ����д�Ų��ױ���
D.X���⻯���Z���⻯�ﷴӦ����һ�ֶ����ȶ��Ļ�����
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ������������ȷ���ǣ�������
A��������һ�����н���Ԫ�أ�������һ��ֻ���зǽ���Ԫ��
B��ij����Ԫ�ص������Ӻ�ij�ǽ���Ԫ�ص���������ɵ�����һ���Ǵ�����
C��������������ú�һ���γ����ӻ�����
D�������ز����ܴ��ε�ˮ��Һ���û�����������
�ο��𰸣�D
���������
�����Ѷȣ���
3������� [��ѧ����ѡ�����ʽṹ������](15��)
ԭ��������������A��B��C��D��E��F(A��B��C��D��E��F�ֱ����Ԫ�ط���)���ֶ�����Ԫ�ء�Ԫ��A��ԭ�Ӱ뾶�ڶ���������С��Ԫ��C�ĵ����ڿ����к�����࣬ ��
�� ��һ�����Ӳ㣬E�������ڵĸ�Ԫ�ص��ʷе�仯����ͼ(Ԫ�ذ�ԭ����������˳����������)��B��C����Ԫ�طֱ�����A�γɵȵ��ӵ�
��һ�����Ӳ㣬E�������ڵĸ�Ԫ�ص��ʷе�仯����ͼ(Ԫ�ذ�ԭ����������˳����������)��B��C����Ԫ�طֱ�����A�γɵȵ��ӵ�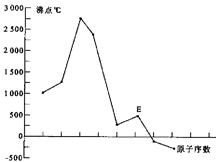 �ס������ַ��ӣ�������
�ס������ַ��ӣ�������
�����и�ԭ�ӵĸ������±���
| ������ | �� | �� |
| ԭ�Ӹ����� | B��A=1��4 | C��A=1��3 |
 ����ҵȾ����
����ҵȾ���� ��?����
��?���� )?��Ԫ�صĵ�һ������(
)?��Ԫ�صĵ�һ������( )(�<����>����=��)��
)(�<����>����=��)���ο��𰸣���1��1s22s22p63s23p5��2�֣���2�� ��������?��2�֣�? sp3��2�֣�
��3�����Ӿ��壨2�֣� ���� ��2�֣���4�����Ӿ��壨2�֣� 6��2�֣�
��5������1�֣�
�����������
�����Ѷȣ���
4������� (8��)A��B��C��D��E����Ԫ�����ڱ���ǰ20��Ԫ�أ�ԭ��������������B��C��Dͬ���ڣ���A��Dͬ���壬E������Ԫ�ؼȲ���ͬ����Ҳ����ͬ���壬B��C��D������������ˮ����������Ͼ��ܷ�����Ӧ�����κ�ˮ��
����������Ϣ���ش��������⣺
(1)A��D�⻯���У��е�ϵ͵���?(ѡ�A����D��)��A��B�������У��뾶��С����?(�����ӷ���)��
(2)Ԫ��C��Ԫ�����ڱ��е�λ����?��
(3)A��E��������ӻ�����侧��(�������ھ����о��д����Ե���С�ظ���Ԫ)�ṹ����ͼ��ʾ��������(�á���ʾ)λ�ڸ�������Ķ�������ģ�������(�á�������ʾ)��λ��С���������ġ��û�����ĵ���ʽ��?��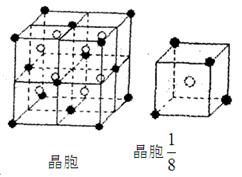
�ο��𰸣�(1)D? Na+?(2)�������ڡ���A��? (3)  ?(ÿ��2�֣���8��)
?(ÿ��2�֣���8��)
�������������Ԫ�صĽṹ�����ʿ�֪��A��B��C��D��E�ֱ���F��Na��Al��Cl��Ca��
��1����������Ӵ�����������Էе�����Ȼ���ġ���������Ų���ͬ�����������뾶��ԭ���������������С����˷����Ӱ뾶���������Ӱ뾶��
��2������ԭ��������13�����������ڱ��е�λ���ǵ������ڡ���A�塣
��3�����ݾ����ṹ��֪�����еĸ�������8��1/8+6��1/2��4����������8�������Ի�ѧʽΪCaF2���������Ӽ������Ե���ʽΪ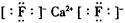 ��
��
�����Ѷȣ�һ��
5��ѡ���� ���з��������ں��м��Լ��ķǼ��Է��ӣ��ҷ����и�ԭ������㶼����8�����ȶ��ṹ���ǣ�������
A��CH4
B��PCl3
C��SiCl4
D��XeF4
�ο��𰸣�A��CH4�����к��еĹ��ۼ��Ǽ��Թ��ۼ�����Hԭ�Ӳ�����8�����ȶ��ṹ����A����
B��PCl3�����к��еĹ��ۼ��Ǽ��Թ��ۼ�������ṹ���Գ��Ǽ��Է��ӣ���B����
C��SiCl4�����к��еĹ��ۼ��Ǽ��Թ��ۼ����ṹ�Գ��ǷǼ��Է��ӣ������и�ԭ������㶼����8�����ȶ��ṹ����C��ȷ��
D��XeF4�����к��еĹ��ۼ��Ǽ��Թ��ۼ���Xe�������12�����ӣ���D����
��ѡC��
���������
�����Ѷȣ���