时间:2017-03-03 00:25:05
1、填空题 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。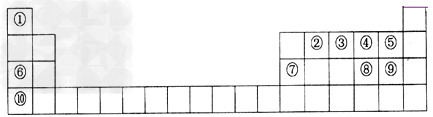
(1)表中最活泼的金属与最活泼的非金属形成的化学式是___________,含有_____键。
(2)⑦号元素的原子结构示意图为___________,其单质既能与酸反应,又能与碱反应,写出与碱反应的化学方程式____________________________________。其最高氧化物对应的水化物与⑥号元素最高价氧化物对应的水化物反应的离子方程式为__________。
(3)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是__________(写化学式),④、⑤、⑧氢化物稳定性由强到弱的顺序是__________(写化学式)。
(4)②和④形成的化合物与④和⑥形成的化合物之间发生氧化还原反应,写出该反应的化学方程式:_______________。
2、选择题 下列元素中,最高正化合价数值最大的是?
[? ]
A、C
B、S
C、F
D、Ne
3、推断题 现有A、B、C、D四种元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B元素与A元素形成的一种化合物为淡黄色固体,该固体遇到空气能生成A的单质;C为原子核内有12个中子的金属元素,当2.4克C与足量热水反应时,在标准状况下放出气体2.24L,C形成正二价阳离子;D元素原子的M层上有7个电子。
(1)写出B、C两种元素的元素符号:B__________,C__________;
(2)画出A2-的离子结构示意图:__________, 指出D在周期表的位置:__________;
(3)写出B的呈淡黄色的化合物与CO2反应的化学方程式:___________________________;
(4)比较D的气态氢化物与H2S和HF的稳定性:____________________(用化学式表示);
(5)用电子式表示C与D形成化合物的过程:____________________。
4、选择题 下列选项中,错误的是
A.酸性:HClO4>HNO3>H3PO4>H2SiO3
B.稳定性:H2S>HCl>HBr>HI
C.金属性:K>Na>Mg>Al
D.气态氢化物的稳定性:H2O>H2S
5、选择题