时间:2017-03-03 00:22:29
1、填空题 下表为元素周期表的一部分,请回答有关问题
(1)?⑤?和?⑧?的元素符号是_________和_________
(2)?此表中最活泼的金属是___________,非金属性最强的元素是___________(填写元素符号)
(3)在?③?~?⑦?元素中,原子半径最大的是________(填写元素符号)。
(4)表中能形成两性氢氧化物的元素是_________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:______________________________;_______________________。
参考答案:(1)Si;Ar
(2)K;F
(3)Mg?
(4)“略”
本题解析:
本题难度:一般
2、选择题 科学家根据元素周期律和原子结构理论预测,原子序数为114的元素称为类铅元素.下面关于它的原子结构和性质预测正确的是
A.类铅元素原子的最外层电子数为5
B.其常见价态为+2、+3、+4
C.它的金属性比铅强
D.它的原子半径比铅小
参考答案:C
本题解析:根据周期表的结构可知,114号元素位于第七周期,第ⅣA,常见化合价是+2和+4价。同主族自上而下原子半径逐渐增大,金属性逐渐增强,所以答案选C。
本题难度:一般
3、选择题 下列叙述正确的是
A.碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱
B.碳族元素的单质都有导电性
C.硅酸的酸性比碳酸的强
D.同一周期中氧族元素比碳族元素的非金属性强
参考答案:D
本题解析:
本题难度:一般
4、选择题 下列各组元素属于p区的是
[? ]
A.原子序数为1、2、7的元素
B.O、S、P
C.Fe、Ar、Cl
D.Na、Li、Mg
参考答案:B
本题解析:
本题难度:简单
5、填空题 看表填空。 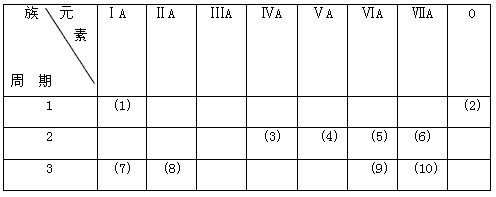
(A) (1)、(5)、(9)号元素,相互化合时可形成两种常见_______化合物,但溶于水后都可以电离出相同的_______离子。
(B)(8)、(10)号元素化合时,可通过_______键形成_______化合物。
(C)(1)、(5)、(7)号元素相互化合形成的物质中,既有_______键,又有_______键。
参考答案:A 共价; 氢
B离子; 离子
C离子; 共价
本题解析:
本题难度:一般