时间:2017-03-03 00:16:15
1、计算题 (8分)28gFe与足量稀盐酸混合,充分反应,消耗多少克HCl?生成FeCl2的物质的量为多少?标准状况下最多能收集到多少升气体?
参考答案:消耗36.5gHCl;生成FeCl2的物质的量为0.5mol;标准状况下最多能收集到11.2L气体。
本题解析:解:Fe + 2HCl = FeCl2 + H2↑
56g 2x36.5g 1mol 22.4L
28g m(HCl) n(FeCl2) V(H2)
m(HCl)=(28x2x36.5)/56=36.5g n(FeCl2)=28x1/56=0.5mol V(H2)=28x22.4/56=11.2L
考点:考查化学反应的计算.
本题难度:一般
2、实验题 用18.4mol/L的浓硫酸稀释成0.92mol/L的稀硫酸100ml,回答下列问题:
(1)
| 应取浓硫酸的体积/ml | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| ? | ? | ? |
参考答案:(1)5.0(2分),100(2分),量筒、烧杯、玻璃棒、胶头滴管(2分)
(2)DECBHG(3分)?(3)AC(3分)
本题解析:(1)用18.4mol/L的浓硫酸稀释成0.92mol/L的稀硫酸100ml,则根据稀释过程中溶质不变可知,需要浓硫酸的体积=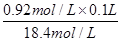 =0.005L=5.0ml,所以应取浓硫酸的体积是5.0ml。配制100ml硫酸,则需要100ml容量瓶。另外还需要量筒量取浓硫酸,稀释浓硫酸用烧杯,稀释和转移还需要玻璃棒,定容时还需要胶头滴管。
=0.005L=5.0ml,所以应取浓硫酸的体积是5.0ml。配制100ml硫酸,则需要100ml容量瓶。另外还需要量筒量取浓硫酸,稀释浓硫酸用烧杯,稀释和转移还需要玻璃棒,定容时还需要胶头滴管。
(2)容量瓶在使用前需要查漏,具体的操作步骤有计算、量取、稀释、冷却、移液、洗涤移液、定容、摇匀等操作,所以其操作顺序是A DECBHGF。
(3)根据cB=nB/V可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大。A、没有将洗涤液转移到容量瓶中,则溶质减少,所配浓度偏低;B、容量瓶洗净后未经干燥处理不会影响实验结果,即浓度不变;C、转移过程中有少量的溶液溅出,则溶质减少,所配浓度偏低;D、摇匀后立即观察,发现溶液未达刻度线,没有再用滴管加几滴蒸馏水至刻度线,浓度不变,因此答案选AC。
本题难度:一般
3、填空题 (12分)实验室配制一定物质的量浓度的溶液,需经计算、称量、溶解、移液、
洗涤、定容、摇匀、装瓶等步骤。现需配制0.2mol/L的CuSO4溶液500mL。
回答下列问题:
(1)用托盘天平称取CuSO4・5H2O晶体的质量是 g。
(2)将溶解并冷却后的溶液转移的过程中用到的玻璃仪器有 。
(3)定容时,加水至距刻度线1-2cm时改用胶头滴管滴加蒸馏水至 。
(4)下列情况会使所配溶液浓度偏低的是 。(填序号)
A定容时俯视
B未将洗涤烧杯后的溶液转移至容量瓶
C加蒸馏水时,不慎超过了刻度线
D砝码上沾有杂质(或者使用生锈的砝码)
E.容量瓶使用前未经干燥
参考答案:(每空2分)
⑴25.0;⑵玻璃棒 烧杯 容量瓶;⑶溶液的凹液面与刻度线相切
⑷BC
本题解析:(1)500mL 0.2mol/L的硫酸铜溶液中含有溶质硫酸铜的物质的量为:0.2mol/L×0.5L=0.1mol,需要CuSO4?5H2O晶体的质量为:250g/mol×0.1mol=25.0g。
(2)溶解并冷却后的溶液转移的过程中用到的玻璃仪器有:盛放溶液的烧杯、引流作用的玻璃棒和500mL容量瓶,故答案为:玻璃棒、烧杯、容量瓶。
(3)定容时,加水至距刻度线1-2cm时改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切。
(4)A、定容时俯视,导致加入的蒸馏水低于容量瓶刻度线,配制的溶液体积偏小,溶液浓度偏高,故A错误;B、未将洗涤烧杯后的溶液转移至容量瓶,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,故B正确; C、加蒸馏水时,不慎超过了刻度线,导致配制的溶液体积偏大,溶液浓度偏低,故C正确;D、砝码上沾有杂质(或者使用生锈的砝码),导致称量的溶质的质量偏大,配制的溶液中溶质的物质的量偏大,配制结果偏高,故D错误;E、容量瓶使用前未经干燥,对溶质的物质的量及溶液的体积都没有影响,所以不影响配制结果,故E错误。
考点:本题考查配制一定物质的量浓度的溶液、误差分析。
本题难度:一般
4、选择题 下列说法正确的是(?)
A.含n molHCl的浓盐酸与足量MnO2反应可生成n NA /4 个氯分子()
B.在密闭容器中建立了N2+3H2 2NH3的平衡,每有17gNH3生成,必有0.5NA个NH3分子分解
2NH3的平衡,每有17gNH3生成,必有0.5NA个NH3分子分解
C.同温同压同体积的CO2和SO2所含氧原子数均为2NA
D.20 g重水(D2O)中含有的电子数为10NA
参考答案:D
本题解析:浓盐酸在和二氧化锰的反应中,浓度会逐渐变稀,而稀盐酸不能和二氧化锰反应,所以选项A中生成的氯气小于n NA /4 个;选项B不正确,因为反应达到平衡状态时正逆反应速率是相等的;选项C不正确,二者不一定都是1mol;20g重水是1mol,含有10mol电子,所以答案选D。
本题难度:一般
5、选择题 在标准状况下,将体积为V?L的A气体,溶于100mL水中,得到密度为ρg?cm-3的溶液,A气体的摩尔质量为M?g?mol-1,则此溶液的物质的量浓度为( )
A.c(A)=
| V?ρ MV+2240 |
| 1000Vρ MV+2240 |
| 1000VρM MV+2240 |
| MV 22.4(V+0.1)ρ |
参考答案:标准状况下V?L的A气体的质量为VL22.4L/mol×M?g?mol-1=VM22.4g
溶液的质量为VM22.4g+100ml×1g/ml=(100+VM22.4)g
所以溶液的质量分数为VM22.4g(100+VM22.4)g=VM2240+VM
所以溶液的物质的量浓度为1000×ρ×VM2240+VMM=1000ρV2240+VMmol/L.
故选:B.
本题解析:
本题难度:简单