时间:2017-03-02 23:55:08
1、选择题 甲溶液的pH为4,乙溶液的pH为2,甲溶液与乙溶液的c(H+)之比为
A.100
B.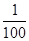
C.2
D.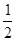
参考答案:B
本题解析:甲溶液的pH为4, c(H+)=10-4mol/L则乙溶液的pH为2, c(H+)=10-2mol/L甲溶液与乙溶液的c(H+)之比为10-4: 10-2=1:100。
考点:离子浓度大小比较。
本题难度:一般
2、选择题 能促进水的电离,并使溶液中c(H+)>c(OH-) 的操作是
[? ]
①将水加热煮沸
②向水中投入一小块金属钠
③向水中通CO2
④向水中通NH3
⑤向水中加入明矾晶体
⑥向水中加入NaHCO3固体
⑦向水中加NaHSO4固体
A .①③⑥⑦
B .①③⑤⑥
C .⑤⑦
D .⑤
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列表述正确的是
A.将 0.1 mol・L-1HCl溶液加热到100℃,溶液的pH仍为1
B.将pH=4的醋酸溶液加水稀释后,溶液中所有离子的浓度均降低
C.常温下,若1mLpH=1的盐酸与10mLNaOH溶液混合后溶液的pH=7,则NaOH溶液的pH=12
D.在滴有酚酞试液的氨水中,加入NH4Cl至溶液呈无色,此时溶液一定显中性
参考答案:C
本题解析:A.盐酸易挥发,将 0.1 mol・L-1HCl溶液加热到100℃,盐酸因挥发c(H+)降低,溶液的pH减小,A项错误;B.将pH=4的醋酸溶液加水稀释后,酸性减弱,c(H+)降低,由于c(H+)・c(OH-)=KwW的乘积不变,溶液中c(OH-)升高,B项错误;C.常温下,若1mLpH=1的盐酸n(H+)=0.0001mol,与10mLNaOH溶液混合后溶液的pH=7,说明酸碱恰好反应,NaOH的物质的量为0.0001mol,则c(NaOH)=0.01mol/L,NaOH溶液的pH=12,C项正确;D.酚酞的变色范围是8-10,PH小于8,呈现无色,在滴有酚酞试液的氨水中,加入NH4Cl至溶液呈无色,此时溶液可能显中性,D项错误;选C。
考点:考查影响电解质溶液的因素,PH的计算,溶液酸碱性的判断。
本题难度:一般
4、选择题 在纯水中存在如下平衡:2H2O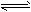 H3O++OH-,若使水的电离平衡向逆反应方向移动,且使溶液中的
H3O++OH-,若使水的电离平衡向逆反应方向移动,且使溶液中的
c(OH-)减小,下列条件能达到的是
[? ]
参考答案:BD
本题解析:
本题难度:一般
5、填空题 (8分)在2 5℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbL NaOH溶液,(题中 a < b, b ≥ 8)。问:
5℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbL NaOH溶液,(题中 a < b, b ≥ 8)。问:
(1)若a+b=14,则Va/Vb= .
(2)若a+b=13,则Va/Vb=
(3)若a+b>14,则Va/Vb= ,且Va Vb(填“>”“<”“=”)
参考答案:(8分)(1)若a+b=14,则Va/Vb= 1:1  .
.
(2)若a+b=13,则Va/Vb=1:10
座位号
本题解析:略
本题难度:一般