时间:2017-03-02 23:28:31
1、填空题 (15分)
工业上以磷肥生产形成的副产物石膏(CaSO4・2H2O)与焦炭为原料可生产硫酸,同时可以得到硫酸钾肥料和氯化钙水合物储热材料。以下是有关的工艺流程示意图。
试回答:
(1)写出方程式:反应Ⅰ___________________________________,
(2)写出方程式:反应Ⅱ______________________________________。
(3)请根据下表和化学平衡知识,分析工业上制硫酸中SO2的催化氧化的适宜条件是
____________________________________。
表Ⅰ:
 ?压?强? / M Pa ?压?强? / M Pa转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
 的方法是___________________________________。
的方法是___________________________________。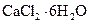 )是目前常用的无机储热材料,选择的依据是___________
)是目前常用的无机储热材料,选择的依据是___________ (填序号)。
(填序号)。参考答案:(15分)
(1)2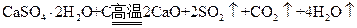 (3分)
(3分)
(2)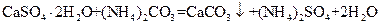 (3分)
(3分)
(反应不写水不扣分)
(3)常压、400―500℃、催化剂的条件下(3分)
(4)取少许滤液滴加到盐酸中产生气泡(3分)
(5)a? d (3分)
本题解析:略
本题难度:一般
2、实验题 工业上采用硫化钠-石灰铁盐法处理高砷废水(砷的主要存在形式为H3AsO3)取得了很好的效果。实现了废水处理过程的“三废”零排放。其主要工艺流程如下: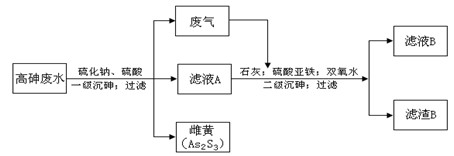
已知:①亚砷酸(H3AsO3)还原性较强,易被氧化为砷酸(H3AsO4)
②亚砷酸盐的溶解性大于相应的砷酸盐[如Ksp(FeAsO3)>Ksp(FeAsO4)]
请回答以下问题:
(1)废气的主要成分为?,通过与石灰发生?反应(填基本反应 类型)被吸收。
类型)被吸收。
(2)写出一级沉砷过程中生成雌黄的离子方程式:?。
(3)滤液A中,除了有Na2SO4、H2SO4以外,还有溶质?。
(4)二级沉砷过程中使用双氧水的目的有?。
A.将三价砷氧化为五价砷,以提高除砷效果
B.将Fe2+氧化可生成Fe(OH) 3沉淀,以加速悬浮物的沉降
C.作绿色氧化剂,不引进新的杂质
(5)过滤操作常用的玻璃仪器有:?
(6)滤渣B的主要成分有?(写两种,用化学式表示)。
参考答案:(10分)(每空2分)
(1)H2S;中和反应(或复分解反应) 2分
(2)2H3AsO3+3S2-+6H+→As2S3↓+6H2O
(或 2H3AsO3+3S2-→As2S3↓+6OH-;H++OH-→H2O)(2分)
(3)H3AsO3(2分)
(4)A B C(少1个选项扣1分,直至扣完)(2分)
(5)漏斗、烧杯、玻璃棒(2分)
(6)FeAsO4 、Ca3(AsO4)2 、Ca3(AsO3)2、Fe(OH) 3 、CaSO4等(合理答案均给2分)
本题解析:略
本题难度:一般
3、选择题 下列有关工业生产的叙述正确的是
A.合成氨生产过程中升高温度可加快反应速率,缩短生产周期,故温度越高越好
B.硫酸工业中,使用催化剂是为了提高SO2转化为SO3的转化率
C.电解精炼铜时,精铜作阴极
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
参考答案:C
本题解析:合成氨过程中温度应该控制在5000C左右,而不是越高越好;硫酸工业中,使用催化剂会加快反应速率,不会提高反应物的转化率;电解饱和食盐水时用离子交换膜法,防止阳极室产生的Cl2进入阴极室。
本题难度:一般
4、选择题 下列变化不属于化学变化的是
A.溶洞的形成过程
B.物质的燃烧
C.合成高分子材料
D.矿石的粉碎
参考答案:D
本题解析:在溶洞的形成过程中,CaCO3变为Ca(HCO3)2,部分Ca(HCO3)2随水流走,部分Ca(HCO3)2又变为CaCO3,形成了石笋、石柱和钟乳石,是化学变化。物质的燃烧,一般是物质跟空气中的氧气发生的反应,有新的物质生成,属于化学变化。合成高分子材料属人工合成新物质,也是化学变化。矿石的粉碎过程中无新物质生成,属物理变化,不是化学变化。
本题难度:简单
5、选择题 20世纪90年代初,国际上提出了“预防污染”的新概念。“绿色化学”是预防污染的基本手段,下列各项中属于“绿色化学”的是:
[? ]
A.处理废弃物
B.杜绝污染源
C.禁食有毒物
D.制定治污规章制度
参考答案:B
本题解析:
本题难度:简单