时间:2017-03-02 23:06:26
1、选择题 下列有关硼元素的叙述中,正确的是
A.从硼的相对原子质量为10.8,可判断硼原子核内中子数为6
B.在三氯化硼分子中,硼原子最外层满足了8电子结构
C.硼元素可以与氢元素结合成氢化物
D.硼元素与氢氧根结合的化合物是一种强碱
参考答案:C
本题解析:从元素的相对原子质量无法确定元素的核内中子数;氯化硼中硼元素最外层有6个电子,未达8电子结构;B(OH)3显弱酸性.
本题难度:一般
2、选择题 下列有关元素性质的递变规律不正确的是
A.Na.Mg.Al的还原性逐渐减弱
B.HCl.PH3.H2S气态氢化物的稳定性逐渐减弱
C.NaOH.KOH的碱性逐渐增强
D.Na.K.Rb的原子半径依次增大
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列叙述不正确的是( )
A.H2S、H2O、HF的稳定性依次增强
B.NaOH、KOH、Mg(OH)2的碱性依次减弱
C.Na、Mg、Al的半径依次减小
D.H2SiO3、H2CO3、H2SO4酸性依次增强
参考答案:A.非金属性:F>O>S,元素的非金属性越强,对应的氢化物越稳定,则H2S、H2O、HF的稳定性依次增强,故A正确;
B.金属性:K>Na>Mg,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则KOH、NaOH、Mg(OH)2的碱性依次减弱,故B错误;
C.同周期元素从左到右原子半径逐渐减小,则Na、Mg、Al的半径依次减小,故C正确;
D.非金属性:S>C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则H2SiO3、H2CO3、H2SO4酸性依次增强,故D正确.
故选B.
本题解析:
本题难度:一般
4、推断题 现有Q、R、X、Y、Z原子序数依次增大的五种短周期元素,短周期的所有元素中Q的原子半径与Z的原子半径之比最小(不包括稀有气体),R、X、Y三种元素的原子核外电子层数相同,同一周期中R的一种单质为黑色固体,Y与Q、R、X、Z均能形成多种常见化合物。
(1)RY2的电子式是______________
(2)比较Q分别与X、Y形成的最简单化合物的稳定性________>_______(用化学式表示)
(3)实验室制取R2Q2的化学方程式是___________________________。
(4)常温下液态化合物甲只含上述元素中的两种,分子中原子个数比1:1,在实验室中用甲可以制取Y的单质化学方程式是_______________________。
(5)电解质乙和丙由上述元素中的几种组成,1mol乙或丙中均含有20mol电子,丙可以抑制乙在水溶液中的电离,则丙中的化学键类型有_______,乙的电离方程式是_____________。
(6)由Q、R两元素形成的含26个电子的气态化合物,该化合物与氧气和KOH溶液可构成燃料电池,写出该燃料电池负极的电极反应式___________。
参考答案:(1)
(2)H2O>NH3
(3)CaC2+2H2O→Ca(OH)2+HC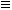 CH↑
CH↑
(4)2H2O2 2H2O+O2↑
2H2O+O2↑
(5)离子键,极性共价健;NH3·H2O NH4++OH-
NH4++OH-
(6)C3H8+26OH--20e-=3CO32-+17H2O
本题解析:
本题难度:一般
5、选择题 下列说法不正确的是
A.同族元素,随着核外电子层数的增加,I1逐渐增大
B.通常情况下,对于同一种元素的原子,其电离能I1
D.I1增大
E.通常情况下,电离 能越小,元素的金属性越强
参考答案:A
本题解析:试题分析:同族元素,随着核外电子层数的增加,I1逐渐减小,故A错误,为本题的正确答案;通常情况下,对于同一种元素的原子,其电离能I1<I2<I3,故B正确;同周期元素,总体变化趋势是随着核电荷数的增加,I1增大,故C正确;通常情况下,电离能越小,元素的金属性越强,故D正确。
考点:元素周期律
点评:本题考查了元素周期律的知识点,该知识点是高考考查的重点和热点,本题属于对基础知识的考查,本题比较容易。
本题难度:困难