时间:2017-03-02 22:53:36
1、选择题 下列关于金属晶体的叙述正确的是( )
A.常温下,金属单质都以金属晶体形式存在
B.金属离子与自由电子之间的强烈作用,在一定外力作用下,不因形变而消失
C.钙的熔沸点低于钾
D.温度越高,金属的导电性越好
参考答案:B
本题解析:常温下,金属单质不都是以金属晶体形式存在的,例如汞在常温下呈液态,故A错误;金属离子与自由电子之间的强烈作用,在一定外力作用下,不因形变而消失,故B正确,为本题的答案;钙的熔沸点高于钾,故C错误;温度越高,金属的导电性越差,故D错误。
点评:本题考查了金属晶体,该考点是高考常考的考点,本题难度不大,本题要记忆的是汞是一种比较特殊的金属,因为其在常温下呈现液体。
本题难度:一般
2、选择题 测知氯化钠晶体中相邻的Na+离子与Cl-离子的距离为a cm,该晶体密度为ρg/cm3,则阿伏加德罗常数可表示为
A.0.585/4a3ρ
B.58.5/8a3ρ
C.58.5/2a3ρ
D.117/a3ρ
参考答案:C
本题解析:氯化钠晶胞中含有4个氯化钠,所以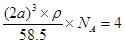 ,解得NA=58.5/2a3ρ,答案选C。
,解得NA=58.5/2a3ρ,答案选C。
本题难度:一般
3、选择题 物质的熔沸点高低能用键能大小解释的是
A.Na > K
B.O2> N2
C.H2O > H2S
D.SiO2 > CO2
参考答案:A
本题解析:A.钠的金属键强于钾的金属性,所以熔沸点:Na>K,与键能有关,故A正确;
B.由于氧气的相对分子质量大于氮气,因此范德华力较大,因此熔沸点:O2>N2,与键能无关,故B正确;C.由于水中含有氢键,H2S中没有氢键,使得水的熔沸点变大,氢键不属于化学键,与键能无关,故C错误;D.SiO2是原子晶体,CO2是分子晶体,所以熔沸点:SiO2>CO2,与键能无关,故D错误;故选A。
本题难度:简单
4、选择题 下列说法中正确的是
A.元素的非金属性越强,其单质的活泼性一定越强
B.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
C.分子晶体的熔沸点低,常温下均呈液态或气态
D.含有金属阳离子的晶体一定是离子晶体
参考答案:B
本题解析:A错,元素的非金属性越强,其单质的活泼性不一定越强,如N与P,N的非金属性比P强,但是N2的活泼性比P弱;B正确;C错,分子晶体的熔沸点低,但常温下不一定均呈液态或气态;D错,如金属晶体;
本题难度:一般
5、选择题 如图是CaF2晶胞的结构.下列说法正确的是( )
A.一个CaF2晶胞中含有8个Ca2+
B.一个CaF2晶胞中含有8个F-
C.在CaF2晶胞中Ca2+的配位数为4
D.在CaF2晶胞中F-的配位数为8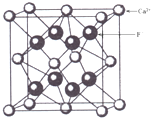
参考答案:B
本题解析:
本题难度:简单