时间:2017-03-02 22:47:39
1、选择题 25℃、101kPa下,碳、氢气和甲烷的燃烧热依次是393.5 kJ·mol—1、285.8 kJ·mol—1
和890.3kJ·mol—1,下列选项中正确的是
A.2H2(g)+O2(g)=2H2O(l)△H=—285.8kJ·mol—1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890.3kJ·mol—1
C.H2(g)+1/2O2(g)=H2O(g)△H<—285.8kJ·mol—1
D.C(s)+2H2(g)=CH4(g)△H=—74.8 kJ·mol—1
参考答案:D
本题解析:燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物.碳单质、氢气、甲烷的热化学方程式分别为:①C(S)+O2(g)═CO2(g)△H=-393.5kJ·mol-1;②H2(g)+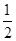 O2(g)═H2O(l)△H=-285.8kJ·mol-1;③CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ·mol-1,根据盖斯定律解答,2H2(g)+O2(g)=2H2O(l)?△H=—571.6kJ·mol—1,A选项错误;甲烷燃烧是放热,应该是△H=-890.3kJ·mol—1,B选项错误;液态水变为气态水,要吸收一部分热量,所以△H>—285.8kJ·mol—1;C选项错误;根据盖斯定律③-(①+②×2)得CH4(g)=C(S)+2H2(g),故△H=(-890.3KJ·mol-1)-[(-393.5KJ·mol-1)+(-285.8kJ·mol-1)×2]=+74.8KJ·mol-1,D选项正确。
O2(g)═H2O(l)△H=-285.8kJ·mol-1;③CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ·mol-1,根据盖斯定律解答,2H2(g)+O2(g)=2H2O(l)?△H=—571.6kJ·mol—1,A选项错误;甲烷燃烧是放热,应该是△H=-890.3kJ·mol—1,B选项错误;液态水变为气态水,要吸收一部分热量,所以△H>—285.8kJ·mol—1;C选项错误;根据盖斯定律③-(①+②×2)得CH4(g)=C(S)+2H2(g),故△H=(-890.3KJ·mol-1)-[(-393.5KJ·mol-1)+(-285.8kJ·mol-1)×2]=+74.8KJ·mol-1,D选项正确。
本题难度:一般
2、选择题 下列溶液一定呈中性的是(?)
A.c(OH-) = 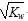 的溶液
的溶液
B.pH=7 的溶液
C.c(H+) =10-14的溶液
D.加甲基橙呈黄色的溶液
参考答案:A
本题解析:A、kw=c(H+)c(OH-), c(OH-) = 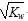 ,故溶液为中性;
,故溶液为中性;
B、如果不在25℃,该溶液不为中性,
C、该溶液可能为碱性;
D、甲基橙的变色范围为3.1~4.4,大于4.4为黄色。
本题难度:简单
3、选择题 下图为对15 mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图像,根据图像推出X (mol/L)和Y (mol/L)的物质的量浓度是下表内各组中的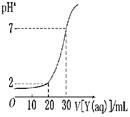
| 选项 | A | B | C | D |
| c(X)/mol·L-1 | 0.035 | 0.070 | 0.03 | 0.06 |
| c(Y)/mol·L-1 | 0.070 | 0.035 | 0.06 | 0.03 参考答案:B 本题解析:滴定过程中pH增大,所以是用氢氧化钠滴定盐酸。恰好中和时0.030×Y=0.015×X,当加氢氧化钠溶液20mL时,pH为2,此时盐酸过量,所以0.015X-0.02Y=0.035×0.01,解得Y=0.035、X=0.07。 本题难度:简单 4、选择题 下列说法不正确的是( ) 参考答案:A、由2H2(g)+O2(g)=2H2O(l)△H=-571.6?kJ/mol,可知1mol氢气完全燃烧生成稳定的氧化物放出的热量为285.8KJ,所以氢气的燃烧热△H=-285.8?kJ/mol,故A正确; 本题解析: 本题难度:简单 5、选择题 下列热化学方程式错误的是(注:△H的绝对值均正确) 参考答案:AD 本题解析: 本题难度:简单 |