ʱ��:2017-03-02 22:46:00
1������� �����裨Si3N4����һ�������մɲ��ϣ������ڸ����µĵ���������ʯӢ�뽹̿ͨ�����·�Ӧ�Ƶã�3SiO2(s) + 6C(s) + 2N2��g�� Si3N4(s) + 6CO(g) + Q��Q>0��
Si3N4(s) + 6CO(g) + Q��Q>0��
���������գ�
��1��ij�¶��¸÷�Ӧ��һ�ݻ�Ϊ2L���ܱ������н��У�2min��ﵽƽ�⣬�պ���2mol���ӷ���ת�ƣ���2min�ڷ�Ӧ������Ϊ��v(CO) = ?���÷�Ӧ��ƽ�ⳣ������ʽΪ������������������?��
��2��������������ʱ������ѹǿ����?��
a��Kֵ��С��ƽ�����淴Ӧ�����ƶ�?
b��Kֵ����ƽ��������Ӧ�����ƶ�
c��Kֵ���䣬ƽ�����淴Ӧ�����ƶ�?
d��Kֵ���䣬ƽ��������Ӧ�����ƶ�
��3��һ����������˵��������Ӧ�Ѵ�ƽ�������������?��
a��c(N2 ) : c(CO) = 1��3? b��3v(N2 ) = v(CO)
c�������������ٸı�? d�������ܶȲ��ٸı�
�ﵽƽ���ı�ijһ��������Ӧ����v��ʱ��t�Ĺ�ϵ��ͼ��ʾ��?
�����ı�N2��CO��������ͼ��t4ʱ����仯��ԭ������� ?��ͼ��t6ʱ����仯��ԭ�������?��
��ͼ��֪��ƽ��������CO������ߵ�ʱ�����?��
�ο��𰸣���1��0.25mol/L��min��1�֣������λ�������֣���?K=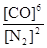 ��1�֣���2��c?��1�֣�
��1�֣���2��c?��1�֣�
��3��c��d��1�֡�2��33�������¶Ȼ���С���������ѹǿ����1�֣��������˴�����1�֣���
t3��t4��1�֣���
�����������1�����淴Ӧ3SiO2��s��+6C��s��+2N2��g��?Si3N4��s��+6CO��g����ƽ�ⳣ��k=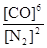 �÷�ӦΪ���ȷ�Ӧ�������¶�ƽ���淴Ӧ���У���ѧƽ�ⳣ����С����2���ɷ���ʽ��֪���÷�Ӧ����Ӧ���������ʵ�������ķ�Ӧ�����Ҷ�������ֵ���ʡ�S��0���ʴ�Ϊ��������3��A����λʱ������2Ħ��Si3N4��ͬʱ����1Ħ����N2������2Ħ��Si3N4������4molN2�������������������������ʲ���ȣ���Ӧδ��ƽ��״̬����A����B��ƽ��ʱc��N2����c��CO��֮��Ϊ1��3�����ܴ���ƽ��״̬��Ҳ���ܲ�����ƽ��״̬���뵪����ת���ʵ��йأ���B����C��ƽ��ʱƽ����ϵ����ֵĺ������䣬CO�İٷֺ������ֲ��䣬˵������ƽ��״̬����C��ȷ��D����λʱ������1Ħ��SiO2��ͬʱ����2Ħ����C������1Ħ��SiO2��Ҫ����2molC��C����������������������ȣ���Ӧ��ƽ��״̬����D��ȷ����ѡCD����4�������ı�N2��CO��������ͼ��֪��t4ʱ˲�������淴Ӧ������ƽ�����淴Ӧ�ƶ����ı�����Ϊ�����¶Ⱥ�ѹ���������ѹǿ��t6ʱ˲�������淴Ӧ������ƽ�ⲻ�ƶ�����Ӧ�Ǽ��������t2ʱ�ı�ı�������ƽ��������Ӧ�ƶ�����t3ʱ���µ���ƽ�⣬t4ʱ�ı�������ƽ�����淴Ӧ�ƶ���t5ʱ�ɴ�ƽ�⣬��t3��t4ƽ��״̬CO�ĺ�����ߣ��ʴ�Ϊ�������¶Ⱥ�ѹ���������ѹǿ�����������t3��t4��
�÷�ӦΪ���ȷ�Ӧ�������¶�ƽ���淴Ӧ���У���ѧƽ�ⳣ����С����2���ɷ���ʽ��֪���÷�Ӧ����Ӧ���������ʵ�������ķ�Ӧ�����Ҷ�������ֵ���ʡ�S��0���ʴ�Ϊ��������3��A����λʱ������2Ħ��Si3N4��ͬʱ����1Ħ����N2������2Ħ��Si3N4������4molN2�������������������������ʲ���ȣ���Ӧδ��ƽ��״̬����A����B��ƽ��ʱc��N2����c��CO��֮��Ϊ1��3�����ܴ���ƽ��״̬��Ҳ���ܲ�����ƽ��״̬���뵪����ת���ʵ��йأ���B����C��ƽ��ʱƽ����ϵ����ֵĺ������䣬CO�İٷֺ������ֲ��䣬˵������ƽ��״̬����C��ȷ��D����λʱ������1Ħ��SiO2��ͬʱ����2Ħ����C������1Ħ��SiO2��Ҫ����2molC��C����������������������ȣ���Ӧ��ƽ��״̬����D��ȷ����ѡCD����4�������ı�N2��CO��������ͼ��֪��t4ʱ˲�������淴Ӧ������ƽ�����淴Ӧ�ƶ����ı�����Ϊ�����¶Ⱥ�ѹ���������ѹǿ��t6ʱ˲�������淴Ӧ������ƽ�ⲻ�ƶ�����Ӧ�Ǽ��������t2ʱ�ı�ı�������ƽ��������Ӧ�ƶ�����t3ʱ���µ���ƽ�⣬t4ʱ�ı�������ƽ�����淴Ӧ�ƶ���t5ʱ�ɴ�ƽ�⣬��t3��t4ƽ��״̬CO�ĺ�����ߣ��ʴ�Ϊ�������¶Ⱥ�ѹ���������ѹǿ�����������t3��t4��
�����Ѷȣ�����
2������� �������ϰ�װ��Ч��ת��������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯����������Ӧ�����������ʣ���������β����Ⱦ��
��1����֪��N2(g)+ O2(g)="2NO(g)" ��H=��180.5 kJ/mol?
2C(s)+ O2(g)="2CO(g)" ��H="-221.0" kJ/mol
C(s)+ O2(g)=CO2(g) ��H="-393.5" kJ/mol
β��ת���ķ�Ӧ֮һ��2NO(g)+2CO(g)=N2(g)+2CO2(g)?��H��?��
��2��ij�о���ѧϰС���ڼ�����Ա��ָ���£���ij�¶�ʱ������������̽��ij�ִ��������µķ�Ӧ���ʣ������崫������ò�ͬʱ���NO��COŨ�������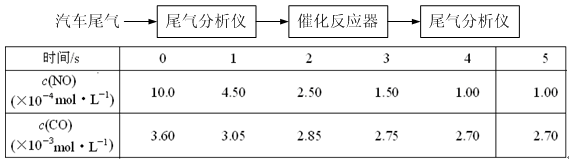
��ش���������(���������¶ȱ仯�Դ�����Ч�ʵ�Ӱ��)��
��ǰ2s�ڵ�ƽ����Ӧ����v (N2) = ___________________��
���ڸ��¶��£���Ӧ��ƽ�ⳣ��K =?����ֻд����������
�۶��ڸÿ��淴Ӧ��ͨ���ۺϷ���������Ϣ�����ٿ���˵��?������ĸ����
A���÷�Ӧ�ķ�Ӧ���Ϻ�ܲ��ȶ�
B���÷�Ӧһ���������ں̵ܶ�ʱ�������
C���÷�Ӧ��ϵ�ﵽƽ��ʱ������һ�ַ�Ӧ��İٷֺ�����С
D���÷�Ӧ��һ�����������Է�����
E���÷�Ӧʹ�ô������岻��
��3��CO��������ȼ�ϵ��Ϊ����ԭ������װ����ͼ��ʾ���õ���е����Ϊ�����ƣ������ƣ�����O2-�����ڹ������NASICON�������ƶ�������˵���������?��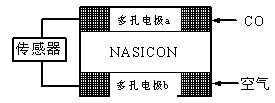
A�������ĵ缫��ӦʽΪ��CO+O2���D2e-��CO2
B������ʱ�缫b��������O2-�ɵ缫a����缫b
C������ʱ�����ɵ缫aͨ������������缫b
D����������ͨ���ĵ���Խ��β����CO�ĺ���Խ��
�ο��𰸣���1��-746.5 kJ/mol(2)��1.88��10��4 mol/(L��s) 5000?��BCD?��3��B
�����������
�����Ѷȣ���
3������� ��12�֣�һ���¶��£���һ�̶�����������У�ͨ��һ������CO��H2O��
�������·�Ӧ��CO (g) ʮH2O (g)  ?CO2 (g) ʮ H2 (g) �� ��H��0
?CO2 (g) ʮ H2 (g) �� ��H��0
��1����850��ʱ��CO��H2OŨ�ȱ仯������ͼ���� 0��4min��ƽ����Ӧ����v(CO2)��?_mol��L-1��min-1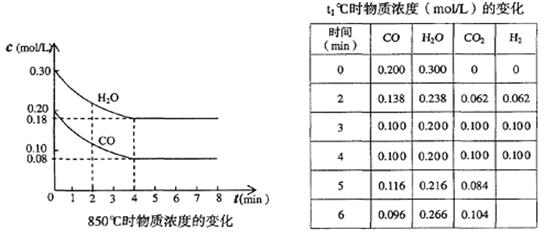
��2��t1��ʱ������ͬ�����з���������Ӧ�������ʵ�Ũ�ȱ仯�����ϱ���
�� ����t1��÷�Ӧ��ƽ�ⳣ��ΪK = ?��
�� t1��ʱ����Ӧ��5min��6min�䣬ƽ��?�ƶ������������һ� �������ڵ�5���Ӹı�һ�������ﵽ��6���ӵ�Ũ�ȣ��ı��������?________��
��3��t2��ʱ����ѧ��ӦCO (g) + H2O (g)  ?CO2 (g) + H2 (g)��ƽ��Ũ�ȷ���c��CO2����c��H2����2 c��CO����c��H2O������t2��?850��,�ж������ǣ�??
?CO2 (g) + H2 (g)��ƽ��Ũ�ȷ���c��CO2����c��H2����2 c��CO����c��H2O������t2��?850��,�ж������ǣ�??
�ο��𰸣���1��0.03 ?��2���� 0.5? �� ���ң�?��H2O (g)Ũ�����ӵ�0.286 mol��L-1��д����H2O (g)Ũ�ȵ�1�֣� ��3���� ��? t2���ƽ�ⳣ��Ϊ2������850���ƽ�ⳣ��1��ƽ������
�����������1����Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ������ͼ���֪����0��4min��CO��Ũ�ȱ仯����0.20mol/L��0.08mol/L��0.12mol/L�����ݷ���ʽ��֪CO2��Ũ�ȱ仯��Ҳ��0.12mol/L�����Է�Ӧ������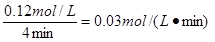 ��
��
��2���ٸ��ݱ������ݿ�֪��Ӧ���е�3minʱ�����ʵ�Ũ�ȾͲ��ٷ����仯����Ӧ�ﵽƽ��״̬������ƽ�ⳣ��Ϊ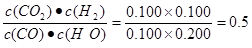 .
.
�ڷ�Ӧ��5min��6min��ʱ����Ӧ���Ũ�Ƚ��ͣ��������Ũ������˵��ƽ��������Ӧ�����ƶ��������ڵ�6minʱCO��Ũ�ȼ�С��H2O��Ũ������CO2��Ũ��Ҳ����˵���ı��������������ˮ������Ũ�ȣ�����CO�ı仯����֪���ڵ�5minʱ��H2O (g)Ũ�����ӵ�0.266mol/L��0.116mol/L��0.096mol/L��0.286 mol��L-1��
��3��ƽ��Ũ�ȷ���c��CO2����c��H2����2 c��CO����c��H2O�������ʱƽ�ⳣ��Ϊ2�����ݣ�1���ɼ����850��ʱ��ƽ�ⳣ��Ϊ1������ʱ����850���ƽ�ⳣ����˵����Ӧ������Ӧ�����ƶ�������Ϊ��Ӧ�Ƿ��ȷ�Ӧ�������¶Ƚ��Ͳ���������Ӧ�����ƶ���
�����Ѷȣ�һ��
4������� 2L�ݻ�������ܱ������У�����1.0molA��2.2molB���������·�Ӧ��
A��g��+2B��g��?C��g��+D��g����
�ڲ�ͬ�¶��£�D�����ʵ���n��D����ʱ��t�Ĺ�ϵ��ͼ
�Իش��������⣺
��1��800��ʱ��0-5min�ڣ���B��ʾ��ƽ����Ӧ����Ϊ______��
��2�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�ı�־��______��
A������ѹǿ����B�����������c��A������
C��2v����B��=v�棨D��D��c��A��=c��C��
E����������ƽ�����������ٸı�F����������ܶȲ���
G��A��B��C��D=1��2��1��1
��3������ͼ�����ݼ���800��ʱ��ƽ�ⳣ��K=______��B��ƽ��ת����Ϊ��______��
�÷�ӦΪ______��Ӧ�������Ȼ���ȣ���
��4��800��ʱ����һ2L�ݻ�������ܱ������У����ijʱ�̸����ʵ������£�
n��A��=2.2mol��n��B��=5.2mol��n��C��=1.8mol��n��D��=1.8mol�����ʱ�÷�Ӧ______���У��������Ӧ�������淴Ӧ������ƽ��״̬������
�ο��𰸣���1��800��ʱ��0-5min�ڣ�D��ƽ����ѧ��Ӧ����v(D)=��nV��t=0.6mol2L5min=0.06mol/Lmin��ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�����v��B����v��D��=2��1=v��B����0.06mol/Lmin��v��B��=0.12mol?L-1?min-1��
�ʴ�Ϊ��0.12mol?L-1?min-1��
��2���÷�Ӧ�Ƿ�Ӧǰ�����������С�ķ�Ӧ����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯��
A���÷�Ӧ�Ƿ�Ӧǰ�����������С�ķ�Ӧ����ѹǿ����ʱ�������ʵ�Ũ�Ȳ��ٷ����仯����A��ȷ��
B����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯����B��ȷ��
C��2v����B��=v�棨D��������֮�Ȳ����ڻ�ѧ������֮�ȣ���Ӧδ��ƽ��״̬����C����
D�����۷�Ӧ�Ƿ�ﵽƽ��״̬��c��A��=c��C�������Բ�����Ϊ�ж�ƽ��״̬�����ݣ���D����
E����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ������䣬�������������䣬���Ի�������ƽ�����������ٸı䣬��������Ϊ��ѧƽ��״̬���ж����ݣ���E��ȷ��
F�����������غ㣬���۷�Ӧ�Ƿ��ƽ��״̬��������������䣬������������䣬���Ի��������ܶ�ʼ�ղ��䣬���Բ�����Ϊ��ѧƽ��״̬���ж����ݣ���F����
G����Ӧ����n��A����n��B����n��C����n��D��=1��2��1��1���У���ʼn��A����n��B������1��2������ƽ���n��A����n��B����n��C����n��D��һ������1��2��1��1����G����
�ʴ�Ϊ��ABE
��3��A��g��+2B��g�� C��g��+D��g����
C��g��+D��g����
��ʼ 1.0mol 2.2mol 0 0
��Ӧ0.6mol1.2mol 0.6mol0.6mol
ƽ��0.4mol 1.0mol 0.6mol0.6mol
ƽ��ʱA��B��C��D�����ʵ�Ũ�ȷֱ�Ϊ0.2mol/L��0.5mol/L��0.3mol/L��0.3mol/l��
��ѧƽ�ⳣ��K=0.3mol/L��0.3mol/L0.2mol/L��(0.5mol/L)2=1.8��mol?L-1��-1��
B��ƽ��ת����=1.2mol2.2mol��100%=54.5%��
����ͼ��֪�������¶ȣ�D�ĺ������٣�����ƽ�����淴Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ��
�ʴ�Ϊ��1.8��mol?L-1��-1��54.5%�����ȣ�
��4��A��B��C��D�����ʵ�Ũ�ȷֱ�Ϊ1.1 mol/L��2.6 mol/L��0.9 mol/L��0.9 mol/L
Ũ����QC=0.9mol/L��0.9mol/L1.1mol/L��(2.6mol/L)2=0.11��mol?L-1��-1��1.8��mol?L-1��-1�����Է�Ӧ������Ӧ������У�
�ʴ�Ϊ��������Ӧ����
���������
�����Ѷȣ�һ��
5�������� ��6�֣���ͼ��ʾ��A�г���1 mol X ��1 mol Y����B�г���2 mol X��2? mol Y����ʼʱ��v��A��=v��B��="a" L������ͬ�¶Ⱥ��д��������£��������и��Է���������Ӧ��X+Y 2Z+W����X��Y��Z��W��Ϊ���壩����ӦΪ���ȷ�Ӧ���ﵽƽ��ʱ��v��A��="1.2a" L��
2Z+W����X��Y��Z��W��Ϊ���壩����ӦΪ���ȷ�Ӧ���ﵽƽ��ʱ��v��A��="1.2a" L��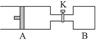
�Իش�
��1��A��X��ת���ʦ�(A)_______________________________________________________��
��2��A��B��X��ת���ʵĹ�ϵ����(A) ___________��(B)��(�������������=��)
(3)��K��һ��ʱ���ִﵽƽ�⣬A�����Ϊ___________L������ͨ��������������ƣ�
�ο��𰸣�(1)40%? (2)��? (3)2-6a
���������X+Y 2Z+W? ��V
2Z+W? ��V
1? 1 ?2? 1? 1
��Ӧ? 0.2a? 0.2a
��ӦǰX�����Ϊ0.5a����Ӧ��0.2a�����(A)=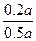 ��100%=40%��
��100%=40%��
A�����Bѹǿ��С��ƽ�����Ʀ�(A)����(B)��
�����Ѷȣ���