时间:2017-03-02 22:45:41
1、选择题 如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
A.湿润淀粉KI试纸未变蓝说明SO2的氧化性弱于I2
B.沾有KMnO4溶液滤纸、湿润的品红试纸均褪色证明了SO2漂白性
C.湿润的蓝色石蕊试纸先变红后褪色
D.NaOH溶液可用于除去实验中多余的SO2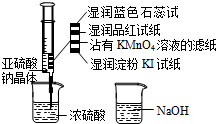
2、填空题 某教师在课堂上用右图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.请答下列问题:
(1)通过试管乙中发生的______
现象说明了铜和浓硫酸发生了化学反应,
并且该现象还能说明产生的气体具有______性.
(2)写出试管甲中所发生反应的化学方程式,并标明电子转移方向和数目______.
(3)试管乙口部浸有碱液的棉花的作用是______,此防范措施也说明产生的气体是______(填“酸性”、“中性”或“碱性”)气体,______(填“有”或“无”)毒性.
(4)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论.为进一步研究酸雨的成分,该同学取某一时段的这种雨水V?L,加入0.5mol/L的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00mL?Ba(OH)2溶液.请计算:
①该雨水中共溶解SO2的体积是______mL(标准状况).
②若生成沉淀物的质量为4.50g,则沉淀物的组成为______(填写化学式).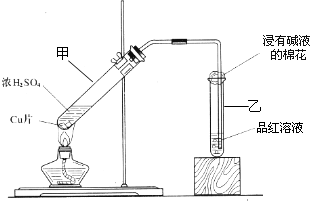
3、选择题 化学与人类生活密切相关.关于下列物质的使用不合理的是( )
A.二氧化硫常用于食品增白
B.碳酸氢钠常用于焙制糕点
C.氯气常用于自来水的杀菌消毒
D.氢氧化铝常用于治疗胃酸过多
4、选择题 将某些化学知识用图象表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,正确的是
[? ]
A.SO2气体通入氯水中 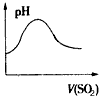
B.醋酸加水稀释 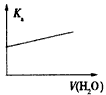
C.硫酸铝溶液中加入过量的氢氧化钡溶液 
D.Cl2通入NaOH溶液中 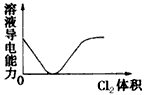
5、填空题 现有?A.二氧化硅?B.三氧化二铁?C.?二氧化硫?D.三氧化二铝。?请你根据已有的知识,选择合适的物质,用字母代号填空:?
(1)能形成酸雨的是________?;
(2)光纤制品的基本原料__________?;
(3)属于两性氧化物的是___________;
(4)红棕色固体是?_____________?。