时间:2017-03-02 22:35:45
1、选择题 下列的各种说法中,正确的是
A.12C的相对原子质量为12g・mol-1
B.MgCl2的摩尔质量是95 g
C.0.5 mol氢元素约含6.02×1023个氢原子
D.32g O2和O3的混合物中,共有2mol氧原子
参考答案:D
本题解析:相对原子质量的单位是1,A错;摩尔质量的单位是g・mol-1,B错;物质的量适用于微观粒子不适用于宏观物质,元素属于宏观物质,C错;32g O2和O3的混合物氧原子的质量是32g,物质的量为32g÷16 g・mol-1=2mol,D对。
考点:常见物理量的单位,物质的量的使用和有关物质的量的计算。
本题难度:一般
2、计算题 (8分)在m L b mol・L-1 AlCl3溶液中,加入等体积a mol・L-1的NaOH溶液。?
(1)当a≤3b时,生成Al(OH)3沉淀的物质的量是___________mol。?
(2)当a、b满足_____________条件时,无沉淀生成。
(3)当a、b满足________?___条件时,有沉淀生成且溶液中无Al3+存在,生成Al(OH)3沉淀的物质的量是________ mol 。
。
参考答案:31.(8分)(1)ma/3? (2)a≥4b? (3)3b≤a<4b ,m(4b-a)
本题解析:分析本题时,写出AlCl3和NaOH反应的方程式,3NaOH+AlCl3=Al(OH)3+3NaCl、4NaOH+AlCl=NaAlO2+3NaCl+2H2O,然后利用铝离子和氢氧根离子以物质的量之比为1:3,恰好沉淀,1:4,沉淀恰好溶解,找出临界值把范围分为三部分进行讨论。
(1)在化学反应中,参加反应的物质的物质的量之比=化学计量数之比。AlCl3和NaOH反应,3NaOH+AlCl3=Al(OH)3+3NaCl,
当AlCl3和NaOH恰好反应即物质的量之比为1:3时,生成的Al(OH)3?物质的量最大.当a≤3b时,反应中NaOH不足量,计算时应以NaOH为标准进行,设生成Al(OH)3沉淀的物质的量为x。
3NaOH+AlCl3=Al(OH)3+3NaCl?
3? 1
m×a? x
3:1=m×a:x
解得?x=ma/3 mol
(2)AlCl3和NaOH反应生成Al(OH)3,Al(OH)3是两性氢氧化物,能够溶于NaOH溶液,所以生成的沉淀会减少,NaOH+Al(OH)3=NaAlO2+2H2O,方程式3NaOH+AlCl3=Al(OH)3+3NaCl和?NaOH+Al(OH)3=NaAlO2+2H2O?相加,得到方程式4NaOH+AlCl=NaAlO2+3NaCl+2H2O,由方程式可得,当AlCl3和NaOH物质的量之比为1:4时,恰好没有沉淀产生.
4NaOH+AlCl=NaAlO2+3NaCl+2H2O?
4? 1
0.05a? 0.05b
a:b=4:1
故答案为:a≥4b;
(3)有沉淀生成且溶液中无Al3+存在,先有沉淀生成,3NaOH+AlCl3=Al(OH)3+3NaCl,后又可能有部分沉淀溶解,NaOH+Al(OH)3=NaAlO2+2H2O,所以3b≤a<4b时,会出现有沉淀生成且溶液中无Al3+存在;当全部生成沉淀时,应以AlCl3为标准进行计算,当沉淀生成后又有部分沉淀溶解时,应以剩余的NaOH为标准进行计算。
设AlCl3全部转化为Al(OH)3时,需要的NaOH为xmol,生成的Al(OH)3为ymol,
3NaOH+AlCl3=Al(OH)3+3NaCl
3? 1? 1
x? mb?y
x=3mb? y=mb
剩余NaOH的物质的量为:ma-3mb,
设生成NaAlO2时需要的Al(OH)3物质的量为zmol,
NaOH+Al(OH)3=NaAlO2+2H2O
1? 1
ma-3mb?z
z= ma-3mb?
所以剩余的Al(OH)3物质的量为mb-(ma-3mb?)=4mb-ma。
故答案为:3b≤a<4b;m(4b-a)。
点评:本题考查的是铝的重要化合物的有关计算及有关计算范围的讨论.在做讨论题时,结合有关化学方程式,找出反应的临界值进行讨论,简洁明了。如:NaOH溶液中通入CO2、向NaAlO2溶液中滴加稀盐酸等都是有关计算范围的讨论。
本题难度:一般
3、选择题 下列选项中的物质所含指定原子数目一定相等的是
A.温度和压强不同,相同质量的N2O和CO2两种气体的总原子数
B.等温等压下,相同体积的C2H4和C2H2、C2H6的混合气体的总原子数
C.等温等压下,相同体积的O2和O3两种气体中的氧原子数
D.相同物质的量、不同体积的NH3和CH4两种气体中的氢原子数
参考答案:A
本题解析:质量相等,N2O和CO2的摩尔质量也相等,则气体的物质的量相等,且两者都是三原子分子,所以它们的总原子数一定相等,A项正确;B项中,碳原子数相等,但是C2H2和C2H6的组成比例不确定,不能判断氢原子数是否相等,B项错误;两种气体的物质的量相等,但两种气体的分子组成不同,故氧原子数不同,C项错误;D项,物质的量相等的NH3和CH4中氢原子数不同,D项错误。
本题难度:一般
4、选择题 若以w1和w2分别表示物质的量浓度为c1 mol・L-1和c2 mol・L-1硫酸溶液的质量分数,已知2 w1=w2,则下列推断正确的(硫酸的密度比纯水的大) ( )
A.2c1=c2
B.2c2=c1
C.c2>2c1
D.c1<c2<2c1
参考答案:C
本题解析:浓硫酸的密度大于水,溶液的浓度越大,密度越大,利用c=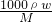 进行判断。设物质的量是浓度为c1 mol?L-1的密度为ρ1,物质的量是浓度为c2mol?L-1硫酸溶液的密度为ρ2,则c1=
进行判断。设物质的量是浓度为c1 mol?L-1的密度为ρ1,物质的量是浓度为c2mol?L-1硫酸溶液的密度为ρ2,则c1=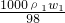 ,c2=
,c2=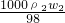 ,
,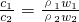 =
=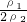 因浓硫酸的密度大于水,溶液的浓度越大,密度越大,则ρ1<ρ2,则c2>2c1,选C.
因浓硫酸的密度大于水,溶液的浓度越大,密度越大,则ρ1<ρ2,则c2>2c1,选C.
考点:考查物质的量浓度与质量分数的计算与比较
本题难度:一般
5、选择题 在100 g浓度为18 mol・L-1,密度为ρ(g・cm-3)的浓硫酸中加入一定量的水稀释成9 mol・L-1的硫酸,则加入水的体积为
A.小于1 00 mL
B.等于100 mL
C.大于100 mL
D.小于 mL
mL
参考答案:A
本题解析:因H2SO4溶液的密度随浓度增大而增大,是一个变值而不是一个定值。设稀释后溶液密度为ρ′,则有:18× ×10-3=9×
×10-3=9×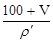 ×10-3, 2
×10-3, 2 =
=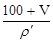 ,因为ρ′<ρ,故V <100(mL)。
,因为ρ′<ρ,故V <100(mL)。
本题难度:一般