表述1??
表述2???
A.
在水中,NaCl的溶解度比I2的溶解度大
NaCl晶体中Cl-与Na+间的作用力大于碘晶体
中分子间的作用力
B.
通常条件下,CH4分子比PbH4分子
稳定性高
Pb的原子半径比C的大,Pb与H之间的键能
比C与H间的小
C.
在形成化合物时,同一主族元素的
化合价相同
同一主族元素原子的最外层电子数相同
D.
P4O10、C6H12O6溶于水后均不导电
P4O10、C6H12O6均属于共价化合物
参考答案:B
本题解析:
本题难度:简单
2、简答题 有A、B、C、D、E、F六种前四周期元素,原子序数A<B<C<D<E<F.A原子只有一个电子层且只含1个电子;B、C两元素的基态原子具有相同能级,且I1(B)>I1(C),其中基态B原子的2p轨道上有3个未成对电子;D原子s电子数比p电子数少4;E原子的3p轨道上得到1个电子后不能再容纳外来电子;F为周期表前四周期中电负性最小的元素.
(1)写出下列元素的元素符号:C______F______
(2)写出E元素原子的价电子轨道表示式______.
(3)B、C两元素原子的电负性大小:B______C(填“<”或“>”).
(4)A2C与A2D的熔沸点:A2C______A2D(填“<”或“>”).
(5)A、C两元素按原子个数比为1:1结合成的化合物化学式为______.
(6)BA3的中心原子杂化方式为______杂化,该化合物的空间构型为______.
参考答案:A、B、C、D、E、F六种前四周期元素,原子序数A<B<C<
本题解析:
本题难度:一般
3、选择题 0.75mol?RO32-共有30mol电子,则R在周期表中的位置是( )
A.第二周期
B.第四周期
C.第ⅣA族
D.第ⅥA族
参考答案:由于0.75mol?RO32-共有30mol电子,
所
本题解析:
本题难度:简单
4、填空题 如图所示每条折线表示周期表ⅣA~ⅦA族中某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是____________,b点代表的是__________。
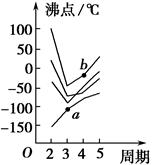
参考答案:SiH4?? H2Se
本题解析:第二周期ⅣA~ⅦA族元素分别是C、N、O、F,其氢化物的沸点由高到低的顺序是
H2O>HF>NH3>CH4,因此,由上至下4条折线分别代表ⅥA、ⅦA、ⅤA、ⅣA族元素的氢化物的沸点变化。那么,b点代表的物质是H2Se,a点代表的物质是SiH4。
本题难度:一般
5、选择题 2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是:
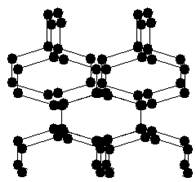
A.该晶体中含有非极性共价键
B.含N5+离子的化合物中既有离子键又有共价键
C.高聚氮与N2、N3、N5、N5+、N60互为同素异形体
D.这种固体的可能潜在应用是烈性炸药或高能材料
参考答案:C
本题解析:
试题分析:A、高聚氮中含N-N键,属于非极性共价键,正确;B、含N5+离子的化合物,为离子化合物,还存在N-N键,则含N5+离子的化合物中既有离子键又有共价键,正确;C、同素异形体的研究对象为单质,而N5+为离子,与单质不能互为同素异形体,错误;D、N-N易断裂,高聚氮不稳定,能量较高,则固体的可能潜在应用是烈性炸药或高能材料,正确。
本题难度:一般