时间:2017-02-07 16:42:17
1、选择题 某容积一定的密闭容器中,可逆反应:A(g)+B(g)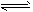 xC(g) △H<0,符合下图所示图象(1)的关系。由此推断对图象(2)的正确说法是
xC(g) △H<0,符合下图所示图象(1)的关系。由此推断对图象(2)的正确说法是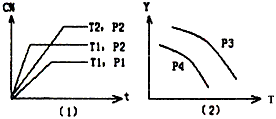 [???? ]
[???? ]
A.P3>P4,Y轴表示A的转化率
B.P3<
C.P3>P4,Y轴表示混合气体密度
D.P3>P4,Y轴表示混合气体的平均摩尔质量
参考答案:AD
本题解析:
本题难度:一般
2、填空题 附加题:2molSO21molO2在一定条件反应:2SO2(g)+O2(g)?2SO3(g)△H<0.若:恒温恒容条件下SO2的转化率为a%;恒温恒压条件下SO2的转化率为b%;恒容绝热条件下SO2的转化率为c%;则它们之间的关系是:(选填:><=条件不够无法确定)
a%______b% a%______c% b%______c%
参考答案:该反应是体积减小,随反应进行气体的物质的量减小,恒温恒压条件
本题解析:
本题难度:一般
3、选择题 在密闭容器中发生如下反应:mA(g)+nB(g) pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍。下列说法中正确的是[???? ]
pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍。下列说法中正确的是[???? ]
A.m+n>p
B.平衡向正反应方向移动
C.A的转化率降低
D.C的体积分数增加
参考答案:C
本题解析:
本题难度:一般
4、选择题 在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是 [???? ]
A.反应混合物的浓度
B.反应体系的压强
C.正、逆反应的速率
D.反应物的转化率
参考答案:D
本题解析:
本题难度:一般
5、填空题 二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)煤的气化的主要化学反应方程式为:___________________________。
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:_________________________________。
(3)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)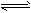 CH3OH(g);ΔH =-90.8 kJ・mol-1
CH3OH(g);ΔH =-90.8 kJ・mol-1
② 2CH3OH(g)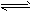 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ・mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ・mol-1
③ CO(g) + H2O(g) CO2(g) + H2(g);ΔH=-41.3 kJ・mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ・mol-1
总反应:3H2(g) + 3CO(g)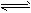 CH3OCH3(g) + CO2(g)的ΔH= ___________;一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是__________(填字母代号)。
CH3OCH3(g) + CO2(g)的ΔH= ___________;一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
参考答案:(1)C+H2O本题解析:
本题难度:一般