ʱ��:2017-02-07 16:16:53
1��ѡ���� һ���¶��£����������Ƶ�����Һ�У����������ܽ�ƽ���ϵ��Ca(OH)2(s) Ca2+ (aq) +2OH- (aq)���������Һ�м��������������Ʒ�ĩ������������ȷ���� [???? ]
Ca2+ (aq) +2OH- (aq)���������Һ�м��������������Ʒ�ĩ������������ȷ���� [???? ]
A����Һ��Ca2+������
B����Һ��c(Ca2+)��С
C����Һ��c(OH-)����
D��pH��С
2��ѡ���� ����˵������ȷ����
A����¯�г�����CaSO4����Na2CO3��Һ���ݺ��ٽ���������ϡ�����ܽ�ȥ��
B��������pH������5��CH3COOH��Һ��NH4Cl��Һ�У�ˮ�ĵ���̶�ǰ�߱Ⱥ��ߴ�
C��BaSO4(s)��4C(s)===BaS(s)��4CO(g)�����²����Է����У�˵���÷�Ӧ�Ħ�H
3�������
ŷ��ԭ����2012��1��1�������պ���̼��˰��Ӧ�Ա����ڻ���ȫ���ů��ʹ�ö���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Եø��ӽ��ȡ������û�ѧ��Ӧԭ�������֪ʶ�о�̼���仯��������ʡ�
��1�����������ҹ���������̼���о�ȡ���ش��չ���õ绡���ϳɵ�̼�����г����д���̼�����������ʣ�������̼���������������������ᴿ���䷴Ӧ�Ļ�ѧ����ʽΪ��???
____C+____K2Cr2O7+?____?��?_____CO2��+_____K2SO4?+?____?Cr2(SO4)3+____H2O
����ɲ���ƽ������ѧ����ʽ��
������������ʽ�ϱ���÷�Ӧ����ת�Ƶķ�������Ŀ��
��2���״���һ������ȼ�ϣ��״�ȼ�ϵ�ؼ�����ʵ��������ҵ����������ҵ��һ����CO��H2Ϊԭ�Ϻϳɼ״����÷�Ӧ���Ȼ�ѧ����ʽΪ��
CO��g��+?2H2��g��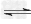 CH3OH��g��?��H1����116?kJ��mol-1
CH3OH��g��?��H1����116?kJ��mol-1
�����д�ʩ������������÷�Ӧ�ķ�Ӧ���ʵ���_________��
A����ʱ��CH3OH�뷴Ӧ��������???
B�����ͷ�Ӧ�¶�
C��������ϵѹǿ?????????????????????????
D��ʹ�ø�Ч����
����֪��??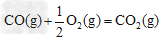 ��H2����283?kJ��mol-1???
��H2����283?kJ��mol-1???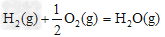 ��H3����242?kJ��mol-1
��H3����242?kJ��mol-1
���ʾ1mol��̬�״�ȼ������CO2��ˮ����ʱ���Ȼ�ѧ����ʽΪ?___________??��
�����ݻ�Ϊ1L�ĺ��������У��ֱ��о���230�桢250���270�������¶��ºϳɼ״��Ĺ��ɡ���ͼ�����������¶��²�ͬ��H2��CO����ʼ��ɱȣ���ʼʱCO�����ʵ�����Ϊ1mol����COƽ��ת���ʵĹ�ϵ��
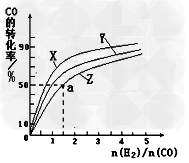
 ???CH3OH��g����ƽ�ⳣ��K?=___________?��
???CH3OH��g����ƽ�ⳣ��K?=___________?��4��ѡ���� ��֪CuSO4��Һ�ֱ���Na2CO3��Na2S��Һ�ķ�Ӧ������£�
| CuSO4 +Na2CO3 | ��Ҫ�� Cu2+ + CO32- + H2O �� Cu(OH)2�� + CO2�� |
| ��Ҫ�� Cu2+ + CO32-�� CuCO3����������������Ӧ�� | |
| CuSO4 +Na2S | ��Ҫ�� Cu2+ + S2- =" " CuS�� |
| ��Ҫ�� Cu2+ + S2- + 2H2O = Cu(OH)2�� + H2S����������������Ӧ�� �ݴ��жϣ����м�������Ksp��С�ıȽ�����ȷ���� A��CuS <Cu(OH)2<CuCO3 B��Cu(OH)2<CuS< CuCO3 C��CuCO3<Cu(OH)2<CuS D��CuCO3< CuS < Cu(OH)2 5��ѡ���� ����ˮ�μӵ�ʢ��AgCl��Һ���Թ��У�AgCl���ܽ⣬�ټ���NaBr��Һ�ֲ�����dz��ɫ���������������̣�����������������ȷ���� [???? ] |