时间:2017-02-07 16:06:58
1、填空题 K2FeO4(高铁酸钾)在水处理、绿色高能电池制备、有机合成等方面都有广泛应用前景。K2FeO4本身的稳定性较差,在水溶液中发生反应:4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑ 研究人员在保持pH约
为9.40的水溶液中对K2FeO4的稳定性研究结果如下图所示。 
图1:K2FeO4浓度为1×10-3 mol/L
图2:K2FeO4浓度为1×10-3 mol/L,加入的另一溶质浓度为0.02 mol/L,空白指未加其它试样(a-磷酸钠 b-草酸钠 c-空白 d-醋酸钠)
图3:K2FeO4浓度为1×10-3 mol/L,加入的另一溶质浓度为5×10-4 mol/L,空白指未加其它试样。
请据此回答下列问题:
(1)由图1可知,在保持pH约为9.40时,升高温度,K2FeO4的稳定性_________(填“增加”、“降低”或“不影响”)。
(2)由图2可知,在水溶液中分别加入磷酸钠、草酸钠、醋酸钠时,K2FeO4的稳定性顺序为__________________(用图中字母序号填空)。
(3)下图曲线e、f是加入NaCl的K2FeO4试样和空白对照实验所测结果。如果忽略Na+对K2FeO4稳定性的影响,其中加NaCl测得的曲线为_________。 
(4)我国学者提出在浓NaOH溶液(非饱和溶液)中用电化学方法来制备高铁酸盐,电解装置如下图。电解时,阳极的电极式反应为________________________。 
(5)K2FeO4用于处理水时,不仅能消毒杀菌,还能吸附水中的悬浮杂质。请写出K2FeO4的还原产物在水中生成Fe(OH)3的离子方程式________________________。
(6)实验室保存K2FeO4的方法是__________________________。
2、填空题 电解原理在化学工业中有广泛的应用。如图表示一个电解池, 装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。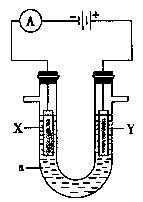
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为 ,在X极附近观察到的现象是 。电解液中向X极方向移动的离子是 。
②Y电极上的电极反应式为 ,
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的电极反应式为 (说明:杂质发生的反应不必写出。)
③溶液中的c(Cu2+)与电解前相比 (填“变大”、“变小”或“不变”)。
3、填空题 (14分)按下图所示装置连接好仪器在U形管中加入饱和氯化铜溶液,用石墨棒作电极,接通电源,电解数分钟后,观察现象。
(1)接电源负极的石墨棒上现象??????????????????电极反应为?????????????????????????????&s.5*u.c.#om???
(2)接电源正极的石墨棒上现象,?????????????????电极反应为???????????????????????????????
电解反应的化学方程式???????????????????????
(3)在上述电解反应中,被氧化的物质是?????????离子
(4)如何验证阳极产生的气体:??????????????????????????
4、计算题 用图所示的装置进行电解。通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。
(1)A中发生反应的化学方程式为????????。
(2)在B中观察到的现象是??????????。
(3)室温下,若从电解开始到结束,A、B装置中共收集到气体0.168 L(标况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求A溶液的pH。
5、填空题 下图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色―红色,碱色―黄色)
回答下列问题:
(1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是________(填编号);
①A管溶液由红变黄 ②B管溶液由红变黄 ③A管溶液不变色 ④B管溶液不变色
(2)写出A管中发生反应的反应式:_____________________________;
(3)写出B管中发生反应的反应式:________________________;
(4)检验a管中气体的方法是____________________;
(5)检验b管中气体的方法是_____________________;
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是__________。