时间:2017-02-07 15:25:15
1、选择题 X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是( )
A.X2Y可能是离子化合物,也可能是共价化合物
B.X与Y的简单离子不可能具有相同的电子层结构
C.X的原子半径一定大于Y的原子半径
D.两元素不可能形成原子个数比为1:1的化合物
参考答案:A、化学式为X2Y的有H2O或Na2O或Li2O,可能是离子
本题解析:
本题难度:简单
2、选择题 下列物质中含离子键的是( )
A.Cl2
B.CO2
C.NaCl
D.CH4
参考答案:C
本题解析:
本题难度:一般
3、填空题 已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大。元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同。
请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)
⑴Y、Z、W元素的第一电离能由大到小的顺序是 ??????????? 。
⑵K的二价离子电子排布式是 ??????????????????? 。
⑶Y、Z元素的某些氢化物的分子中均含有18个电子,则Y的这种氢化物的化学式是 ???????? ;Y、Z的这些氢化物的沸点相差较大的主要原因是 ???????? 。
⑷若X、Y、W形成的某化合物(相对分子质量为46)呈酸性,则该化合物分子中Y原子轨道的杂化类型是 ??????? ;1 mol该分子中含有 σ键的数目是 ??? 。
⑸Z、K两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是 ??????? ,Z原子的配位数是 ???????????? 。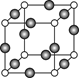
参考答案:⑴N>O>C???⑵[Ar] 3d9???⑶C2H6氮的氢化
本题解析:
试题分析:根据题意可知这几种元素分别是:X是H;Y是C;Z是N;W是O;K是Cu。⑴一般情况下,同一周期的元素,元素的非金属性越强,其失去电子越难,即第一电离能就越大。但是由于N原子的电子处于半充满的稳定状态,所以失去电子比O还难,因此C、N、O元素的第一电离能由大到小的顺序是N>O>C。⑵29号元素Cu的二价离子电子排布式是[Ar] 3d9。(3)具有18个电子的碳元素的氢化物的化学物质为C2H6。具有18个电子的氮元素的氢化物的化学物质为N2H4。C2H6、N2H4的沸点相差较大是因为在乙烷C
本题难度:一般
4、选择题 泽维尔研究发现,当激光脉冲照射NaI时,Na+和I-两核间距1.0~1.5nm,呈离子键;当两核靠近约距
0.28nm时,呈现共价键。根据泽维尔的研究成果能得出的结论是[???? ]
A.NaI晶体是离子化合物和共价化合物的混合物
B.离子化合物中可能含有共价键
C.NaI晶体中既有离子键,又有共价键
D.共价键和离子键没有明显的界线
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列物质中,既有离子键,又有共价键的是( )