时间:2017-02-07 15:17:21
1、选择题 冬季的降雪给机场和马路带来诸多不便,其中醋酸钾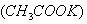 是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是(??? )
是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是(??? )
A.1 mol的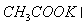 质量为98
质量为98 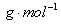
B.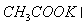 的摩尔质量等于它的相对分子质量
的摩尔质量等于它的相对分子质量
C.一个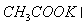 微粒的质量约为
微粒的质量约为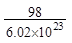 g
g
D.含有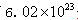 个碳原子的
个碳原子的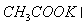 的物质的量为?1 mol?
的物质的量为?1 mol?
参考答案:C
本题解析:质量的单位g,A错误;CH3COOK的摩尔质量当以克为单位时等于它的相对分子质量,B错误;含有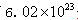 个碳原子CH3COOK的物质的量为0.5mol,D错误。答案选C。
个碳原子CH3COOK的物质的量为0.5mol,D错误。答案选C。
本题难度:一般
2、填空题 (11分)(1)在标准状况下,将???????L NH3溶于水得到0.5 L 0.5 mol・L-1的氨水;配制100 mL 0.1mol・L-1 CuSO4溶液,需要CuSO4・5H2O于???????g。取出5 mL该溶液,它的物质的量浓度为????????,该100 mL溶液可以跟浓度为0.1 mol・L-1?的NaOH溶液???????mL完全反应。
(2)在H、O、H+、H2、OH-、H2O六种微粒中,保持氢气化学性质的微粒是(填化学式,下同)???????;电解水时变化的最小微粒是???????;水变成水蒸气时???????没有变化;带电的微粒是???????;质子数多于核外电子数的微粒是???????。
(3)有相同状况下的两种气体12C18O和14N2。若两种气体的质量相等,则12C18O和14N2气体所含质子数之比为???????;若两种气体的分子数相同,则12C18O和14N2的体积之比为???????。
参考答案:本题解析:略
本题难度:一般
3、选择题 下列有关0.2mol・L-1BaCl2溶液的说法不正确的是
[???? ]
参考答案:A
本题解析:
试题分析:
A、0.2mol?L-1 BaCl2溶液中氯离子的物质的量浓度为0.4mol/L,与溶液的体积无关,故A错误;
B、0.2mol?L-1 BaCl2溶液中钡离子的物质的量浓度为0.2mol/L,与溶液的体积无关,故B正确;
C、N=nNA=CVNA=0.2mol?L-1×0.5L×2×NA=0.2NA,故C正确;
D、N=nNA=CVNA=0.2mol?L-1×0.5L×3×NA=0.3NA,故D正确。
故选A.
本题难度:简单
4、选择题 设NA为阿伏加德罗常数,下列说法正确的是(???)
A.1mol Cl2通入水中,充分反应后转移电子数为NA
B.常温下,1.12L NO2气体含分子数为0.05NA
C.1L 0.5mol・L-1碳酸氢钠溶液中含离子数为NA
D.通常状况下16gO2和O3混合气体中含氧原子数为NA
参考答案:D
本题解析:
试题分析:A、Cl2+H2O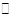 HCl+HClO,反应为可逆反应,有限度的所以Cl2只能部分与水反应,错误;B、标准状况下,1.12L气体的物质的量才是0.05mol,错误;C、溶液中的H2O、HCO3-要发生电离,错误;D、16gO2和O3混合气体相当于16g的O,M(O)=16g/mol,所以含氧原子数
HCl+HClO,反应为可逆反应,有限度的所以Cl2只能部分与水反应,错误;B、标准状况下,1.12L气体的物质的量才是0.05mol,错误;C、溶液中的H2O、HCO3-要发生电离,错误;D、16gO2和O3混合气体相当于16g的O,M(O)=16g/mol,所以含氧原子数
本题难度:一般
5、选择题 把500mL有BaCl2和KCl的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为( )
A.0.1(b-2a)mol/L
B.10( 2a-b)mol/L
C.10(b-2a)mol/L
D.10(b-a)mol/L
参考答案:C
本题解析:
试题分析:混合溶液分成两等份,每份溶液浓度相同.一份加入含a mol 硫酸钠的溶液,发生反应Ba2++SO42-=BaSO4↓,恰好使钡离子完全沉淀,可知该份中n(Ba2+)=(Na2SO4)=amol;另一份加入含bmol 硝酸银的溶液,发生反应Ag++Cl-=AgCl↓,恰好使氯离子完全沉淀,则n(Cl-)=n(Ag+)=bmol,根据电荷守恒可知每份中2n(Ba2+)+n(K+)=n(Cl-),每份溶液中n(K+)=bmol-2amol=(b-2a)mol,故钾离子浓度为(b-2a)mol/0.1L=10(b-2a)mol?L-1,故C项正确。
考点:本题考查离子反应的有关计算。
本题难度:一般