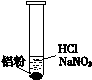
ⅰ. 实验初始,未见明显现象
ⅱ. 过一会儿,出现气泡,有刺激性气味
?
为确认“刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
① 刺激性气味的气体是______。
② 产生该气体的离子方程式是______。
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是______。
(5)实验结果证实:NO3?在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物。习题中的无色溶液一定能大量存在的是Na+和OH-。
2、填空题 (10分)
(1)铝是一种重要的金属材料,铝热反应可以焊接钢轨,请写出铝在高温下与三氧化二铁反应的化学方程式???????????????????????
(2)某铝合金中含有合金元素镁、铜、硅,为了测定合金中铝的含量,设计了如下实验,请回答有关问题:
①称取样品ag,将样品溶于足量的稀盐酸,过滤;
②滤液中加入过量的氢氧化钠溶液,过滤,有关的离子方程式为:?????????????????
③步骤②的滤液中通过足量的CO2气体,可产生Al(OH)3沉淀
④步骤③过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称量,其质量为bg,原样品中铝的质量分数为???????????
(3)工业上,硅是在电炉中用炭粉还原二氧化碳硅制得的,写出该反应的化学方程式
????????????????????????????????????,若往电炉中加入12g二氧化硅和足量炭粉的混合物,生成的气体在标准状况下的体积为????????????????。
3、选择题 下列有关物质的性质和该性质的应用均正确的是( )
A.晶体硅具有半导体性质,可用于生产光导纤维
B.二氧化硫有漂白性,可用于加工食品使食品增白
C.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸
D.铝具有良好导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料
4、选择题 下列有关结构和性质的说法中,正确的是( )
A.由于铝在常温下不能与氧气反应,所以铝制品具有一定的抗腐蚀性能,是一种应用广泛的金属材料
B.住FeCl3溶液中滴入KI一淀粉溶液,溶液变蓝色
C.元素非金属性Cl>S的实验依据是酸性HCl>H2S
D.同周期主族元素的原子形成的简单离子的电子层结构一定相同
5、填空题 某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
实验步骤
| 实验现象
| ①将打磨过的铝片(过量)放入一定浓度的CuCl?2溶液中。
| 产生气泡,析出疏松的红色固体,溶液逐渐变为无色。
| ②反应结束后分离出溶液备用。
| ?
| ③红色固体用蒸馏水洗涤后,置于潮湿空气中。
| 一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3]。
?
按实验中发生反应的现象写出下列化学方程式(是离子反应的只写离子方程式)
①析出疏松的红色固体????????????????????????????????????????????????;
③一段时间后固体由红色变为绿色??????????????????????????????????????。
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。持续电解,在阴极附近的溶液中还可观察到的现象是????????????????????????????????????????????????????????????????????????????。
解释此现象的离子方程式是???????????????????????????、????????????????????????????????。
(3)工业上可用铝与软锰矿(主要成分为MnO2)反应来治炼金属锰。
①用铝与软锰矿冶炼锰的原理是(用化学方程式表示)
???????????????????????????????????????????????????????????????????。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是???????????????????????????????????????????????????????????????????。
|
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
|