时间:2017-02-02 07:10:42
1、选择题 室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是(? )
A.0.1 mol/L的盐酸和0.1 mol/L的氢氧化钠溶液
B.0.1 mol/L的盐酸和0.1 mol/L的氢氧化钡溶液
C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液
D.pH=4的盐酸和pH=10的氨水
参考答案:BD
本题解析:本题考查了酸碱反应后溶液pH的计算及判断。HCl为一元强酸,NaOH为一元强碱,Ba(OH)2为二元强碱,故等体积等物质的量浓度的HCl与NaOH恰好中和,pH=7,而与Ba(OH)2反应时 ,Ba(OH)2过量,pH>7,故A错误,B正确;pH=4的醋酸溶液中电离出的c(H+)=1×10-4 mol/L,pH=10的NaOH溶液电离出的c(OH-)=1×10-4 mol/L,因此仅CH3COOH电离出的H+恰好与NaOH中和,还有大量的CH3COOH分子过量,故pH<7,同理,D项中氨水过量较多,溶液显碱
本题难度:一般
2、选择题 在25℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5kJ/mol、285.8kJ/mol、870.3kJ/mol,则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为???????????? ( )
A.-488.3 kJ/mol
B.+488.3 kJ/mol
C.-191 kJ/mol
D.+191 kJ/mol
参考答案:A
本题解析:由题意可知:C(s)+O2(g)=CO2(g);ΔH=-393.5 kJ/mol ①
H2(g)+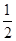 O2 (g)=H2O(l);ΔH=-285.8 kJ/mol ②
O2 (g)=H2O(l);ΔH=-285.8 kJ/mol ②
CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l);ΔH=-870.3 kJ/mol ③
①×2+②×2-③即得:
本题难度:一般
3、选择题 室温下,用0.100 0 mol・L-1NaOH溶液分别滴定体积均为20.00 mL的盐酸和醋酸溶液,滴定曲线如右图。下列说法正确的是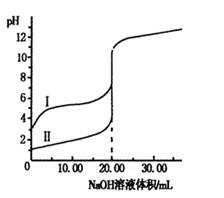
A.I、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.盐酸和醋酸的浓度均为0.100 0 mol・L-1
C.pH=7时,两种酸所消耗NaOH溶液的体积相等
D.V(NaOH)=20.00mL时,c(Cl一)=c(CH3COO一)
参考答案:B
本题解析:
试题分析:A、根据图像可知,曲线发生突变时均消耗20.00ml氢氧化钠溶液,这说明醋酸和盐酸的起始浓度均是0.100 0 mol/L。滴定开始时0.1000mol/L盐酸pH=1,0.1000mol/L醋酸pH>1,所以滴定盐酸的曲线是图Ⅱ,滴定醋酸的曲线是图Ⅰ,故A错误;B、根据A中分析可知,盐酸和醋酸的浓度均为0.100 0 mol/L,故B正确;C、醋酸钠水解呈碱性,氯化钠不水解,pH=7时,醋酸所用NaOH溶液的体积小,故C错误;D、V(NaOH)=20.00?mL?时,二者反应生成氯化钠
本题难度:一般
4、选择题 下列说法不正确的是(????)
A.乙醇做燃料易燃烧,污染小,但不可再生
B.选择燃料需要考虑燃料热值的大小
C.若反应物总能量大于生成物总能量则反应为放热反应
D.将煤制成水煤气提高煤的利用率
参考答案:A
本题解析:乙醇做燃料易燃烧,污染小,可再生。
本题难度:简单
5、填空题 燃烧热
(1)反应热可分为__________、__________、__________等,其中以跟__________相关的__________实际应用较广。
____________________,叫做该物质的燃烧热。单位为__________。燃烧热通常可利用仪器由实验测得。
(2)选择燃料应从物质的燃烧热、燃料的__________、__________、__________、__________、__________、对__________的影响等方面综合考虑。
参考答案:(1)燃烧热?中和热?溶解热?燃料品质?燃烧热? 25 ℃、
本题解析:反应热通常是指:体系在等温、等压过程中发生物理或化学的变化时所放出或吸收的热量。化学反应热有多种形式,如:生成热、燃烧热、中和热、溶解热等。其中燃烧热实际应用较广泛;在101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热.单位为kJ/mol;选择燃料应从物质的燃烧热、燃料的储量?开采?运输?储存的条件?价格?生态环境等因素考虑。
本题难度:简单