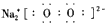1
2
O2(g)═SO3(g)△H=-98.32kJ/mol现有4molSO2参加反应,当放出314.3kJ热量时,SO2的转化率最接近于( )
A.40%
B.50%
C.80%
D.90%
参考答案:C
本题解析:
本题难度:一般
3、选择题 不管化学反应过程是一步完成还是分为数步完成,这个过程的热效应是相同的。
已知:H2O(g)===H2O(l) ΔH1=-Q1 kJ·mol-1①
C2H5OH(g)===C2H5OH(l) ΔH2=-Q2 kJ·mol-1②
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-Q3 kJ·mol-1③
若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
A.(Q1+Q2+Q3) kJ
B.[0.5(Q1+Q2+Q3)] kJ
C.(0.5Q1-1.5Q2+0.5Q3) kJ
D.(1.5Q1-0.5Q2+0.5Q3) kJ
参考答案:D
本题解析:
试题分析:根据盖斯定律,将【③式+②式-(3×①式)】就得到46克酒精液体完全燃烧,最后恢复到室温的情况,将ΔH数值代入计算即可知道D选项正确。
考点:盖斯定律的应用
点评:掌握盖斯定律的概念。
本题难度:一般
4、填空题 SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一。
(1)在接触法制硫酸的过程中,发生2SO2(g)+O2(g)  2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题: 2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:

①平衡状态由A到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”);
②将2.0molSO2和1.0molO2置于10L的密闭容器中,若40s后反应达到平衡,此时体系总压强为0.10MPa,这一段时间内SO2的平均反应速率为 。
该反应的平衡常数为 。
(2)用CH4催化还原NOx可消除氮的氧化物的污染,例如:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol—1
取标准状况下4.48LCH4并使之完全反应:
①若将NO2还原至N2,整个过程中转移电子的物质的量为 ;
②若还原NO2和NO的混合物,放出的总热量Q的取值范围是 。
参考答案:(1)①=;(1分)②0.0040mol·L-1·s-1,8
本题解析:
试题分析:(1)平衡常数只受温度的影响,温度不变,则压强不变,平衡状态由A变到B时,则k(A)=k(B);(2)由图象知,体系总压强为0.10MPa时SO2的平衡转化率为0.8,则
2SO2(g)+O2(g) 2SO3(g) 2SO3(g)
起始:2.0mol 1.0mol 0
转化:1.6mol 0.8mol 1.6mol
平衡:0.4mol 0.2mol 1.6mol
则平衡时:c(SO2)=0.04mol/L,c(O2)=0.02mol/L,c(SO3)=0.16mol/L,SO2的平均反应速率为1.6mol/10L/40s=0.0040mol·L-1·s-1,K=c(SO3)2/c(SO2)2·c(O2)=(0.16)2/(0.04)2×0.02=800;(2)①CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H="-1160kJ/mol" 利用盖斯定律将①+②/2可得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ/moln(CH4)=4.48L/22.4L/mol=0.2mol,整个过程中转移的电子总数为:0.20mol×8=1.60mol,放出的热量为:0.2mol×867kJ/mol=173.4kJ。②上述可知,若反应物中全部是为二氧化氮,放出的热量为173.4kJ。根据盖斯定律可据算出若全部为一氧化氮放出热量为232kJ,故放出的热量范围是173.4kJ<Q<232kJ。
考点:盖斯定律,化学平衡常数,化学平衡。
本题难度:困难
5、选择题 下列化学用语正确的是
[???? ]
A.表示乙炔“燃烧热”对应的热化学方程式:C2H2 (g)+ O2(g)=2CO2(g)+H2O(g) △H =-1 256kJ/mol
B.Na2O2的电子式: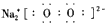
C.电解氢氧化钠溶液铁作电极,阳极的电极反应式为:Fe-3e-+3OH-=Fe(OH)3
D.表示中和热的热化学方程式:NaOH( aq)+ H2SO4(aq)=Na2SO4(aq)+H2O(l) △H=- 57. 3kJ/mol
参考答案:D
本题解析:
本题难度:一般
|