时间:2017-02-02 06:56:41
1、选择题 用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是(??)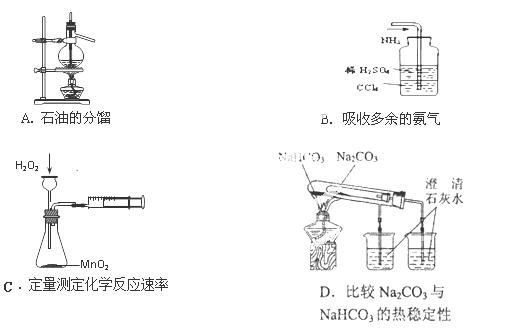
2、选择题 下列实验方案能达到预期目的的是
①实验室保存FeCl3溶液应加少量稀盐酸,并且放入少量的Fe粉
②氢氧化钠溶液保存在配有橡胶塞的细口瓶中
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有SO42-
④用丁达尔现象可以区分食盐水和淀粉溶液
⑤工业上可用金属铝与V2O5在高温下冶炼矾,铝作还原剂
A.①②④
B.①②⑤
C.②④⑤
D.②③④
3、选择题 下列说法中不正确的是?
①用稀盐酸清洗做焰色反应的金属铂丝
②医疗上可用碳酸钡作X射线透视肠胃的内服药
③水玻璃在建筑业用做粘合剂
④铝和铜具有良好的导电性,所以电工操作时,可把铜线和铝线绞接在一起
⑤氯化铵可用于金属的焊接上,以除去金属表面的氧化物薄膜
⑥医用酒精的质量分数为75%
⑦用新制备的Cu(OH)2悬浊液与病人尿液共热,可检验病人尿液中是否含有葡萄糖
A.②③⑦
B.④⑤⑥
C.①③⑤
D.②④⑥
4、填空题 (8分)有一瓶澄清的溶液,其中可能含有K+、Na+、Ba2+、Mg2+、Fe3+、Cl-、CO、SO,取该溶液进行如下实验:
(1)取pH试纸检验,表明溶液呈强酸性,排除________存在。
(2)另取部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,则可排除________、________离子的存在。
(3)取上述碱性溶液加Na2CO3溶液,有白色沉淀生成,可排除________离子的存在。
(4)根据以上实验事实确定:该溶液中肯定存在的离子是________、________;可能存在的离子是________、________。
5、实验题 (11分)某学生需要用0.5mol·L-1的NaCl溶液80mL?,并到实验室进行配制。试回答下列各题。
(1)经计算,应该用托盘天平称取NaCl固体_________g。
(2)若用NaCl固体配制溶液,需使用的玻璃仪器有_________________?? ____________
(3)配制过程有以下操作:A.移液,B.称量,C.洗涤,D.定容,E.溶解,F.摇匀。其正确的操作顺序应是_______________________ (填序号)。
(4)下列操作会导致所得溶液浓度偏低的是______________(填序号)。
A.定容时仰视容量瓶刻度线???????????????????????????
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处