时间:2017-02-02 06:18:05
1、填空题 物质的结构是决定物质性质的重要因素。请回答下列问题:
(1)基态Ni原子核外电子排布式为____________;第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是_________________。
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分为0.069nm和0.078nm,则熔点NiO_____________FeO(填“<”或“>”);NiO晶胞中Ni2+的配位数为____________。
(3)肼可用作火箭燃料,燃烧时发生的反应是:N2O4+2N2H4=3N2+4H2O,若该反应中有4molN―H键断裂,形成的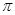 键有________mol。
键有________mol。
参考答案:(8分)(1)1s22s22p63s23p63d84s2(2
本题解析:
试题分析:(1)Ni的原子序数为28,根据构造原理和能量最低原理可写出电子排布式为1s22s22p63s23p63d84s2。第二周期有2个未成对电子的元素是C和O元素,非金属性越强,电负性越大。碳元素的非金属性弱于氧元素,因此电负性较小的是C元素。
(2)Ni2+和Fe2+的离子半径分别为69pm和78pm,离子半径越小,离子键作用力越大,晶体的熔沸点越高,所以熔点NiO>FeO。NaCl中钠离子和氯离子的配位数分别为6,NiO的晶体结构类型与氯化钠的相同,NiO晶胞中Ni和O的配位数分别
本题难度:一般
2、选择题 已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
A.元素A、B组成的化合物常温下一定呈气态
B.工业上常用电解法制备元素C、D、E的单质
C.化合物AE与CE具有相同类型的化学键
D.一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应
参考答案:B
本题解析:
本题难度:简单
3、选择题 下列叙述中正确的是[???? ]
A.在极性分子中不可能存在非极性键
B.在离子晶体中不可能存在极性键
C.在原子晶体中可能存在离子键
D.含有共价键的晶体可能是离子晶体
参考答案:D
本题解析:
本题难度:简单
4、填空题 化合物A是一种不稳定的物质,它的分子组成可用OxFy表示。10 mL A气体能分解生成15 mL O2和10 mL F2(同温同压下)。
(1)A的化学式是____________________,推断依据是____________________。
(2)已知A分子中x个氧原子里……O―O―O……链状排列,则A分子的电子式是__________,结构式为__________。
参考答案:(1)O3F2?阿伏加德罗定律和质量守恒定律
(2)<
本题解析:依题意V(A)∶V(O2)∶V(F2)=10∶15∶10=2∶3∶2,根据阿伏加德罗定律有2A====3O2+2F2,再根据质量守恒定律。A的化学式O3F2。
本题难度:简单
5、选择题 下列分子中,键的极性最强的是 [???? ]
A.PH3
B.HF
C.HBr
D.HCl
参考答案:B
本题解析:
本题难度:简单