时间:2017-02-02 06:09:16
1、选择题 设NA为阿伏加德罗常数,下列关于0.2 mol·L-1Ba(NO3)2溶液的叙述不正确的是(???)
A.2 L溶液中阴、阳离子总数为0.8 NA
B.500 mL溶液中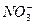 离子浓度为0.2 mol·L-1
离子浓度为0.2 mol·L-1
C.500 mL溶液中Ba2+离子浓度为0.2 mol·L-1
D.500 mL溶液中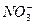 离子浓度为0.2 NA
离子浓度为0.2 NA
参考答案:AB
本题解析:本题主要考查一定物质的量浓度的溶液中粒子数目的求算方法。首先要弄清物质的量浓度和粒子数目的转化关系,即:
物质的量浓度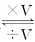 物质的量
物质的量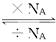 本题难度:简单
本题难度:简单
2、选择题 精确配制一定物质的量浓度的NaOH溶液,下面实验操作正确的是(???)
A.称量时,将NaOH固体放在纸上
B.将称好的NaOH固体放入容量瓶中,加入少量水
C.在烧杯中溶解NaOH固体后,立即将溶液注入容量瓶中
D.将烧杯中已冷却的NaOH溶液注入未经干燥的容量瓶中
参考答案:D
本题解析:逐项分析。A选项NaOH具有吸湿性和腐蚀性,不能直接放在托盘或纸上称量,应放在玻璃器皿中称量;B选项固体物质应在烧杯中溶解,尤其像NaOH固体溶解时放出大量热,会使配得溶液浓度不准确;C选项NaOH溶解后,应将溶液冷却到室温,再转移到容量瓶中,否则会使结果偏大;D选项未经干燥的容量瓶对浓度没有影响。
本题难度:简单
3、选择题 下列叙述正确的是(?????)
A.1 mol H2O的质量为18g/mol
B.标准状况下,1 mol任何物质体积均为22.4L
C.CH4的摩尔质量为16g
D.3.01×1023个SO2分子的质量为32g
参考答案:D
本题解析:
试题分析:质量的单位是g,A不正确;摩尔质量的单位是g/mol,C不正确;B不正确,标准状况下,1 mol任何气体的体积均为22.4L。根据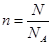 可知,选项D中SO2的物质的量是0.5mol,质量是0.5mol×64g/mol=32g,答案选D。
可知,选项D中SO2的物质的量是0.5mol,质量是0.5mol×64g/mol=32g,答案选D。
点评:该题容易错选C。这是由于不能准确把握气体摩尔体积的
本题难度:一般
4、选择题 NA代表阿伏加德罗常数的数值,下列说法正确的是
A.1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA
B.标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
C.8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA
D.1 mol Na被完全氧化生成Na2O2,失去2 NA个电子
参考答案:A
本题解析:
试题分析:A、1个(-14C1H3)中含有的质子数是6+3=9,中子数是14-6+0=8,所以1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA,正确;B、标准状况下氯仿不是气体,所以11.2L的氯仿的物质的量不是0.5mol,则含有的C-Cl键的数目不是1.5NA,错误;C、8.7g二氧化锰的物质的量是0.1mol,HCl的物质的量是0.4mol,恰好符合二者反应的化学方程式中的物质的量之比,但二氧化锰与稀盐酸不反应,所以实际生成的氯气的物质的量小于0.1mol,则氯气的分子数小于0.1NA,错误;D、Na与氧气反应生成过氧化钠时Na失去1个电子生成+1价钠离子,所以1molNa完全反应失去电子数目是NA,错误,答案选A。
考点:考查阿伏伽德罗常数与微粒数的关系
本题难度:困难
5、选择题 一定量的质量分数为14%的氢氧化钾溶液,若将其蒸发掉100 g水后,其质量分数为28%,体积为125 mL,则浓缩后的KOH的物质的量浓度为
[???? ]
参考答案:B
本题解析:
本题难度:一般