时间:2017-02-02 05:54:11
1、填空题 (1)+3价Co的配合物CoClm・nNH3,中心原子的配位数为6,若1 mol该配合物与足量AgNO3溶液反应生成1 mol AgCl沉淀,用配合物形式写出该配合物的化学式???????????。
(2)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大磁记录性能越好。离子型氧化物MnO2和Fe3O4及Cr2O3中,磁性最大的是___________。
(3)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨(如下左图),每个碳原子通过 ? 杂化与周围碳原子成键。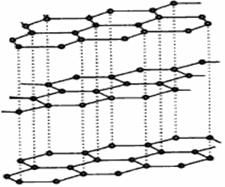 ?
? ?????????????????
?????????????????
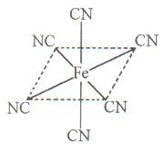
(4)铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如上右图。
①已知CN―与N2结构相似,1molCN-中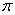 键数目为???????????。
键数目为???????????。
②上述沉淀溶解过程的化学方程式为??????????????????????????????????。
参考答案:(10分)(1)[CoCl2(NH3)4]Cl(2)Fe3O
本题解析:
试题分析:(1)1 mol该配合物与足量AgNO3溶液反应生成1 mol AgCl沉淀,这说明该配位化合物中有1个氯离子不是配体。又因为Cr是+3价的,则氯原子的购书是3个,由于配位数是6,所以化学式应该是[CoCl2(NH3)4]Cl。
(2)根据核外电子排布式可知,离子型氧化物MnO2和Fe3O4及Cr2O3中金属阳离子含有的未成对电子分别是3、14/3、3,所以磁性最大的Fe3O4。
(3)石墨是层状结构,所以每个碳原子通过sp2杂化与周围碳原子成键。
①CN―与N2结构相
本题难度:一般
2、选择题 2010年诺贝尔物理奖授予发现石墨烯的开创性研究者,金刚石、石墨、C60和石墨烯的结构示意图分别如下图所示,下列说法不正确的是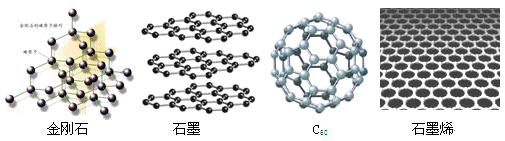
A.金刚石和石墨烯中碳原子的杂化方式不同
B.金刚石、石墨、C60和石墨烯的关系:互为同素异形体
C.这四种物质完全燃烧后的产物都是CO2
D.石墨与C60的晶体类型相同
参考答案:D
本题解析:
答案:D
A.正确,金刚石和石墨烯中碳原子的杂化方式不同,分别是sp3、sp2
B.正确,金刚石、石墨、C60和石墨烯都是由碳元素形成的不同单质,金刚石、石墨、C60和石墨烯的关系:互为同素异形体
C.正确,它们都由碳元素组成,这四种物质完全燃烧后的产物都是CO2
D.不正确,石墨与C60的晶体类型不相同,前者是混合晶体,后者是分子晶体。
本题难度:一般
3、填空题 (5分)有一种蓝色晶体,它的结构特征是Fe2+和Fe3+分别占据立方体互不相邻的顶点,而CN― 离子位于立方体的棱上。
(1)根据晶体结构特点,推出其化学式(用最简单整数示)______________ __。
(2)此粒子带何种电荷?用什么样的离子可与其结合成电中性的物质?写出此电中性物质的化学式(用M+表示)。?????????????????????????????????????????????????
(3)指出(2)中添加离子在晶体结构中的什么位置?
参考答案:(5分,各1分)(1) [FeFe(CN)6] -??? 本题解析: 本题难度:一般 4、简答题 (I)CH3+、CH3-、CH3-都是重要的有机反应中间体,有关它们的说法正确的是______. 参考答案:(1)A.甲烷分子变成CH3+、CH3-、CH3-时,失去的 本题解析: 本题难度:一般 5、判断题 AX4四面体 (A为中心原子,如硅、锗;X为配位原子,如氧、硫) 在无机化合物中很常见。四面体T1按下图所示方式相连可形成一系列“超四面体”(T2、T3・・・): 参考答案:⑴T4超四面体的化学式为A20X35 本题解析:⑴根据连接规律,超四面体中A原子与上一个相邻的超四面体中X原子数相同,所以T4中,A原子数为20,X原子数为20+(10+5)=35,即T4为T20X35 。 本题难度:一般
试题分析:(1)Fe2+、Fe3+占据立方体的互不相邻的顶点,则每个立方体上有4个Fe2+、4个Fe3+,根据晶体的空间结构特点,每个顶点上的粒子有1/8属于该立方体,则该立方体中有1/2个Fe2+、1/2个Fe3+,CN-位于立方体的棱上,棱上的微粒有1/4属于该立方体,该立方体中有3个CN-,所以该晶体的化学式为[FeFe(CN)6]-。
(2)此化学式带负电荷,所以应该均和阳离子才能成为电中性的物质。若结合M+形成中性粒子,此微粒化学式为MFeFe(CN)6。
(3)由于M+离子
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个CH3-或一个CH3+和CH3-结合均可得到CH3CH3
(II)锌是一种重要的金属,锌及其化合物有着广泛的应用.
(1)指出锌在周期表中的位置:______周期,______族,______区.
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式______;葡萄糖分子中碳原子杂化方式有______.
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于______(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在图1中表示[Zn(NH3)4]2+中Zn2+与N之间的化学键.
(4)图2表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为______;该化合物的晶体熔点比干冰高得多,原因是______.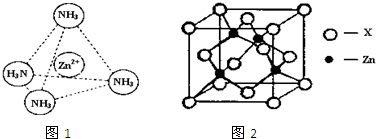
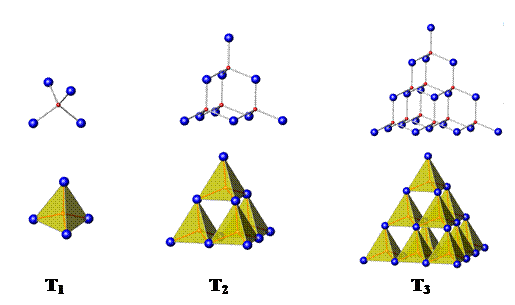
⑴ 上图中T1、T2和T3的化学式分别为AX4、A4X10和A10X20,推出超四面体T4的化学式。
⑵ 分别指出超四面体T3、T4中各有几种环境不同的X原子,每种X原子各连接几个A原子?在上述两种超四面体中每种X原子的数目各是多少?
⑶ 若分别以T1、T2、T3、T4为结构单元共顶点相连(顶点X原子只连接两个A原子),形成无限三维结构,分别写出所得三维骨架的化学式。
⑷ 欲使上述T3超四面体连接所得三维骨架的化学式所带电荷分别为+4、0和-4,A选Zn2+、In3+或Ge4+,X取S2-,给出带三种不同电荷的骨架的化学式(各给出一种,结构单元中的离子数成简单整数比)。
⑵T3超四面体中
⑵T3中,所有X原子都位于超四面体的面上,每个面如下图所示(顶点、交点位置为X原子):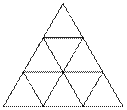
根据该图形的对称性可知:顶点X边接一个A,棱