时间:2017-02-02 05:13:07
1、填空题 工业生产Na2S常用方法是无水芒硝(Na2SO4)一碳还原法,其流程示意图如下:
(1)若煅烧阶段所得气体为等物质的量的CO和CO2。写出煅烧时发生的总反应方程式:______________________。
(2)用碱液浸出产品比用热水更好,理由是__________________。
(3)废水中汞常用硫化钠除去,汞的除去率与溶液pH和硫化钠实际用量与理论用量比值x的关系如图所示。为使除汞达到最佳效果,应控制条件是________________。
(4)取Na2S(含少量NaOH),加入到CuSO4溶液中,充分搅拌,若反应后溶液pH=4,此时溶液中c(S2-)=________mol・L-1[已知:CuS的Ksp=8.8×10-36;Cu(OH)2的Ksp=2.2×10-20(保留2位有效数字)]。
(5)纳米Cu2O常用电解法制备,制备过程用铜棒和石墨棒做电极,Cu(NO3)2做电解液。电解生成Cu2O应在________;该电极pH将________(填“升高”“不变”或“降低”),用电极方程式解释pH发生变化的原因______________________。
2、选择题 将足量的AgI 分别放入下列物质中,AgI 的溶解度由大到小的排列顺序是??[???? ]
①5mL0.001mol・L-1KI溶液
②15mL0.002mol・L-1CaI2
③35mL0.003mol・L-1HI溶液
④15mL蒸馏水
⑤45mL0.005mol・L-1AgNO3
A.①>②>③>④>⑤
B.④>①>③>②>⑤
C.⑤>④>②>①>③
D.④>③>⑤>②>①
3、填空题 科学家利用淡水与海水之间含盐量的差别发明了一种新型电池――水电池。
(1)用二氧化锰纳米棒作电池正极可提高发电效率,这是利用纳米材料的 ?? 特性,使之能与钠离子充分接触。
(2)水电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池的负极反应式为 。水电池工作时,Na+不断向??????极方向移动。
(3)水电池生成1 mol Na2Mn5O10转移电子的物质的量为???。
(4)某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,溶液中金属阳离子的浓度与溶液pH的关系如右图。请据右图分析: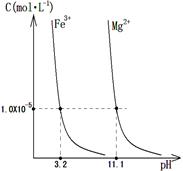
①该温度下,溶度积常数的关系为:KSP[Fe(OH)3]????KSP[Mg(OH)2](填“>”、“=”或“<”);
②如果在新生成的Mg(OH)2浊液中滴入足量的FeCl3溶液,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是??????????????????????????????????????????????????????????????。
4、选择题 25℃时,水的电离达到平衡:H2O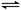 H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
A.向水中加入稀醋酸,平衡逆移,c(H+)降低
B.将水加热,KW增大,pH不变
C.向水中加入少量固体硫酸氢钾,c(H+)增大,KW不变
D.pH=10的NaOH溶液与pH=10的NaClO溶液中,水电离c(H+)之比等于106
5、选择题 查阅资料得知Fe3+、Mg2+、Al3+在浓度均为0.1mol・L-1时,氢氧化物沉淀的pH如下表:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | |
| 开始沉淀的pH | 2.3 | 10.8 | 3.7 | 开始溶解的pH:7.8 |
| 完全沉淀的pH | 4.3 | 12.4 | 5.2 | 完全溶解的pH:10.0 ??????若要从含Fe3+、Mg2+、Al3+的混合溶液中,只得到Fe(OH)3沉淀,则应调节溶液的pH范围A.12.4~14????????? B.7.8~10.0??????? C.10.0~10.8???????? D.3.7~5.2 |