1、选择题 下列实验中颜色变化正确的是(???????)
A.鸡蛋清中加入浓硝酸出现黄色沉淀
B.淀粉溶液中加入KI溶液变蓝色
C.葡萄糖溶液与新制Cu(OH)2浊液混合加热出现砖红色沉淀
D.湿润的PH试纸遇氨气变红色
参考答案:AC
本题解析:
试题分析:鸡蛋清中加入浓硝酸出现黄色沉淀,因为鸡蛋清是含有苯环的蛋白质,含有苯环的蛋白质加入浓硝酸会出现黄色沉淀。A选项正确。淀粉溶液中加入碘单质变蓝色,而KI溶液没有此现象。B选项错误。葡萄糖溶液与新制Cu(OH)2浊液混合加热出现砖红色沉淀。C选项正确。湿润的PH试纸遇氨气呈碱性应变蓝色。D选项错误。
点评:了解教材所提到的典型的实验的操作及现象的描述,是正确解答这类题的基础,所以在学业水平复习时更要回归课本。
本题难度:简单
2、选择题 不用任何试剂就可鉴别的是( )
A.氨水和AlCl3
B.KAlO2和KHSO4
C.FeCl3和KOH
D.Na2CO3和HNO3
参考答案:A、无论将氨水滴到氯化铝溶液中还是将氯化铝溶液滴到氨水中,都
本题解析:
本题难度:一般
3、简答题 亚硫酸钠和硫代硫酸钠(Na2S2O3)都是重要的含硫化合物.某化学兴趣小组进行以下有关实验,填写下列空白.
实验Ⅰ证明Na2SO3中硫元素的价态能发生
+4
S
→+6
S
转化
(1)实验中,不需要用到的试剂有______(填标号).
A.稀硫酸?B.H2O2溶液?C.稀盐酸?D.淀粉碘化钾溶液?E.BaCl2溶液
观察到的现象是______.
实验Ⅱ制取硫代硫酸钠晶体
利用如图所示装置进行实验.已知:①硫代硫酸钠能与酸发生反应
②装置d中发生反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2

(2)装置b中发生反应的化学方程式为______.
(3)装置c的作用是______.
(4)装置d中的反应结束后,先关闭分液漏斗旋塞,接下来的操作是______,待d中溶液冷却后,倒入蒸发皿,蒸发浓缩,冷却、结晶…获得硫代硫酸钠晶体.
实验Ⅲ测定某硫代硫酸钠样品的纯度(设:样品中只含Na2SO3杂质)设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品m?g,配制成250mL待测溶液.
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用n?mol?L-1?I2标准溶液滴定(发生反应:2S2O32-+I2=S4O62-+2I-),至滴定终点.
(5)②中消耗I2标准溶液VmL,样品中Na2S2O3的百分含量为______(用代数式表示).
(6)该实验方案存在的一个明显缺陷是______.
参考答案:(1)证明Na2SO3中硫元素的价态能发生+4价变化为+6价
本题解析:
本题难度:一般
4、实验题 (8分)某课外小组利用H2还原黄色的WO3粉末来测定W的相对原子质量。下图是测定装置的示意图,A中的试剂是盐酸。
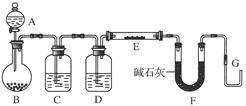
请回答下列问题:
(1)仪器中装入的试剂:B________、C________、D________。
(2)连接好装置后应首先__________________________________________________,其方法是______________________________________________________________________________________________________________________________________。
(3)“加热反应管E”和“从A瓶逐滴滴加液体”这两步操作应该先进行的是
________________________________________________________________________。
在这两步之间还应进行的操作是___________________________________________
________________________________________________________________________。
(4)反应过程中G管逸出的气体是___________________________________________,
其处理方法是___________________________________________________________
________________________________________________________________________。
(5)从实验中测得了下列数据:
①空E管的质量a
②E管和WO3的总质量b
③反应后E管和W粉的总质量c(冷却到室温称量)
④反应前F管及内盛物的总质量d
⑤反应后F管及内盛物的总质量e
由以上数据可以列出计算W的相对原子质量的两个不同计算式(除W外,其他涉及的元素的相对原子质量均为已知)。
计算式1:Ar(W)=________;计算式2:Ar(W)=________。
参考答案:(1)锌粒"水"浓硫酸
(2)检查气密性"将G弯管浸没
本题解析:(1)根据题干实验目的,首先确定B为制取H2的发生装置。应放活泼金属Zn粒,C、D是除气装置分别除H2中的HCl气体和水蒸气。
(2)进行实验前一定检查装置的气密性,检密要注意三步:第一步先封闭气体,第二步对封闭气体改变压强,第三步说出对应现象。
(3)H2在点燃或受热前一定要验纯且尾气也应把它燃烧掉。
本题难度:一般
5、选择题 下列实验不能达到预期目的的是
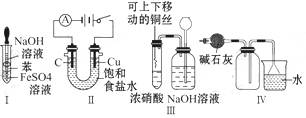
A.利用Ⅰ制取Fe(OH)2
B.利用Ⅱ装置电解饱和食盐水
C.利用Ⅲ装置进行铜与浓硝酸反应的实验
D.利用Ⅳ装置收集NH3
参考答案:B
本题解析:略
本题难度:一般
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G