时间:2017-01-24 19:17:18
1、选择题 有关热化学方程式书写与对应表述均正确的是 [???? ]
A.稀醋酸与0.1?mol/LNaOH溶液反应:H+(aq)+OH-(aq)?=?H2O(l)???△H?=?-57.3kJ/mol
B.氢气的燃烧热为285.5?kJ/mol,?则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)??△H?=?+285.5kJ/mol
C.密闭容器中,9.6?g硫粉与11.?2?g铁粉混合加热生成硫化亚铁17?.6?g时,放出19.12?kJ热量。?则Fe(s)+S(s)=FeS(s)??△H=?-?95.6KJ/mol
D.已知2C(s)+O2(g)=2CO(g)??△H=-221?kJ/mol,则可知C的燃烧热为110.5?kJ/mol
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列说法不正确的是(????)
A.乙醇做燃料易燃烧,污染小,但不可再生
B.选择燃料需要考虑燃料热值的大小
C.若反应物总能量大于生成物总能量则反应为放热反应
D.将煤制成水煤气提高煤的利用率
参考答案:A
本题解析:乙醇做燃料易燃烧,污染小,可再生。
本题难度:简单
3、选择题 有甲、乙两种溶液,甲溶液的pH是乙溶液pH的2倍,则甲、乙两溶液中的C(H+)
A ?2:1??????? B 100:1 ??????????C? 1:100??????????D ?无法确定
参考答案:D
本题解析:略
本题难度:一般
4、选择题 常温下,某溶液中由水电离的c(H+) = 1×10-13mol·L-1,该溶液可能是
①氯化氢水溶液??②氯化铵水溶液?③硝酸钠水溶液??④氢氧化钠水溶液
A.①④
B.①②
C.②③
D.③④
参考答案:A
本题解析:常温下,纯水电离出的c(H+) = 1×10-7mol·L-1,可知,该溶液中水的电离:H2O H++OH-受抑制
H++OH-受抑制
故①提供的H+、④电离出的OH—均可抑制水的电离,答案为A;
而氯化铵由铵根离子水解促进水的电离,硝酸钠对水的电离无任何影响
本题难度:简单
5、选择题 将pH=8的NaOH与pH=10的NaOH溶液等体积混合后,溶液后c(H+)最接近于( )
A.(10-8+10-10) mol/L
B.(10-4+10-6) mol/L
C.(10-8+10-10) mol/L
D.2×10-10 mol/L
参考答案:D
本题解析:
试题分析:将pH=8的NaOH与pH=10的NaOH溶液等体积混合后,溶液中OH-的浓度是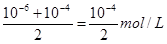 ,则根据水的离子积常数可知c(H+)=
,则根据水的离子积常数可知c(H+)=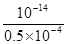 本题难度:简单
本题难度:简单