时间:2017-01-24 19:15:39
1、填空题 (12分)污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。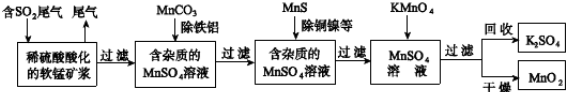
请回答下列问题:
(1)上述流程脱硫实现了 (选填下列字母编号)。
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(2)过滤操作用到的玻璃仪器有: 。
(3)用MnCO3能除去溶液中Al3+和Fe3+,其原因是 。
(4)写出KMnO4溶液加入到MnSO4溶液中制备MnO2的离子反应方程式: ;用惰性电极电解MnSO4溶液也可制得MnO2,其阳极的电极反应式是 。
(5)MnO2是碱性锌锰电池的电极材料,电池反应方程式为:2MnO2+Zn+H2O====2MnOOH+Zn(OH)2,写出该电池放电时,正极的电极反应式是 。
2、选择题 在图中的8个装置中,属于原电池的是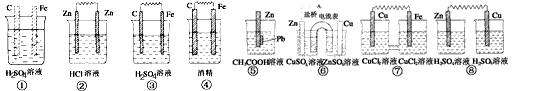 [???? ]
[???? ]
A.①②③⑤⑧ ?
B.③④⑥⑦
C.④⑤⑥⑦? ???
D.③⑤⑦
3、填空题 (10分)有如下两个反应
A:2HCl+Ba(OH)2=BaCl2+2H2O????B:2Fe3++Cu=2Fe2++Cu2+
(1)根据两反应的本质,判断能否设计成原电池:A???????,B????????,(填“能”或“不能”)不能设计成原电池的原因是??????????????????????????????????????????;
(2)根据能设计成原电池的反应选择适合的材料和试剂设计一个原电池
①负极材料是?????????,正极材料是?????????,电解质溶液是???????????????;
②写出负极的电极反应式??????????????????????????????????????????????????;
③若导线上转移电子0.2 mol,则负极质量减少???????????????。
4、填空题 (14分)
已知CO(g)+H2O(g) CO2(g)+H2(g)反应的平衡常数和温度的关系如下:
CO2(g)+H2(g)反应的平衡常数和温度的关系如下:
| |温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 回答下列问题: (1)该反应的△H 0(填“<”“ >”“ =”); (2)830℃时,向一个5 L的密闭容器中充入0.20mol的CO和0.80mol的H2O,反应初始6s内CO的平均反应速率v(CO)="0.003" mol・L-1・s-1,则6S末CO2的物质的量浓度为 ;反应经一段时间后,达到平衡后CO的转化率为 ; (3)判断该反应是否达到平衡的依据为 (填正确选项前的字母); a.压强不随时间改变 b.气体的密度不随时间改变 c.c(CO)不随时间改变 d.单位时间里生成CO和H2的物质的量相等 (4)已知1000℃时,要使CO的转化率超过90%,则起始物c(H2O): c(CO)应不低于 ; (5)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式 ; (6)已知CO可用于制备很多物质: 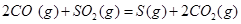 ΔH=+8.0kJ・mol-1 ΔH=+8.0kJ・mol-1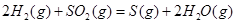 ΔH=+90.4kJ・mol-1 ΔH=+90.4kJ・mol-1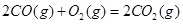 ΔH=-556.0kJ・mol-1 ΔH=-556.0kJ・mol-1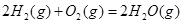 ΔH=-483.6kJ・mol-1 ΔH=-483.6kJ・mol-1请写出 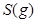 与 与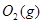 反应生成 反应生成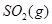 热化学方程式 。 热化学方程式 。 5、实验题 某同学想利用原电池反应检测Zn和Cu的金属活动性顺序。请你帮他选择适宜的材料和试剂设计一个原电池,并完成下列实验报告: |