时间:2017-01-24 19:14:59
1、选择题 下列物质电子式书写正确的是??[???? ]
A.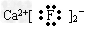 ???????
???????
B.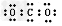 ??????
??????
C.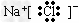 ??????
??????
D. ?
?
2、简答题 (11分)
2-1 画出2,4-戊二酮的钠盐与Mn3+形成的电中性配合物的结构式(配体用 表示)。
表示)。
2-2 已知该配合物的磁矩为4.9玻尔磁子,配合物中Mn的未成对电子数为?????。
2-3 回答:该化合物有无手性?为什么?
2-4 画出2,4戊二酮负离子的结构简式(必须明确其共轭部分),写出其中离域π键的表示符号。
2-5 橙黄色固体配合物A的名称是三氯化六氨合钴(Ⅲ),是将二氯化钴、浓氨水、氯化铵和过氧化氢混合,以活性炭为催化剂合成的。机理研究发现,反应过程中首先得到Co(NH3)62+离子,随后发生配体取代反应,得到以新配体为桥键的双核离子B4+,接着发生桥键断裂,同时2个中心原子分别将1个电子传递到均裂后的新配体上,得到2个C2+离子,最后C2+离子在活性炭表面上发生配体取代反应,并与氯离子结合形成固体配合物A。写出合成配合物A的总反应方程式;画出B4+和C2+离子的结构式。
总反应方程式:
B4+和C2+离子的结构式:
3、填空题 (每空1分,共12分)
H2O 分子构型??????,中心原子采取?????杂化,属于????分子(填极性或非极性)
SO3 分子构型??????,中心原子采取????杂化,属于?????????分子(填极性或非极性)
HCN分子构型???????,中心原子采取????杂化,属于?????????分子(填极性或非极性)
CH4 ?????构型????????,中心原子采取????杂化,属于?????????分子(填极性或非极性)
4、填空题 已知元素X、Y、Z、W、Q均为短周期元素,原子序数依次增大,X基态原子的核外电子分布在3 个能级,且各能级电子数相等,Z是地壳中含量最多的元素,W是电负性最大的元素,元素Q的核电荷数等于Y、W原子的最外层电子数之和。另有R元素位于元素周期表第4周期第Ⅷ族,外围电子层有2个未成对电子,请回答下列问题。
(1)微粒XZ32-的中心原子杂化类型为????????????????化合物YW3的空间构型为??????????????。
(2)R基态原子的电子排布式为????????????????,元素X、Y、Z的第一电离能由大到小的顺序为
?????????????????????????????????????????????????????????????????(用元素符号表示)。
(3)一种新型导体晶体的晶胞如右图所示,则该晶体的化学式为????????????????,其中一个Q原子紧邻????????????????个R原子。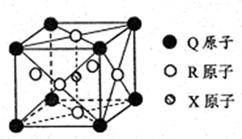
(4)R的氢氧化物能溶于含XY-离子的溶液生成一种配离子[R(XY)4]2-,该反应的离子方程式是??????????弱酸HXY分子中存在的σ键与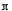 键的数目之比为????????????????。
键的数目之比为????????????????。
5、选择题 下列有关化学键与晶体结构说法正确的是[???? ]
A.两种元素组成的分子中一定只有极性键
B.离子化合物的熔点一定比共价化合物的高
C.非金属元素组成的化合物一定是共价化合物
D.含有阴离子的化合物一定含有阳离子