1、选择题 在标准状况下,用铂电极电解CuSO4溶液,当阴极产生12.8g铜时,阳极放出的气体是(???)
A.1.12LH2
B.1.12LO2
C.2.24LH2
D.2.24LO2
参考答案:D
本题解析:
试题分析:用铂电极电解CuSO4溶液的化学方程式为2CuSO4+ 2H2O  2Cu + 2H2SO4+ O2↑.在整个闭合回路中电子转移数目相等。所以n(Cu)=12.8g÷64g/mol=0.2mol.n(e-)=0.4mol。所以n(O2)=0.1mol.在标准状况下其体积为2.24L。选项为D。
2Cu + 2H2SO4+ O2↑.在整个闭合回路中电子转移数目相等。所以n(Cu)=12.8g÷64g/mol=0.2mol.n(e-)=0.4mol。所以n(O2)=0.1mol.在标准状况下其体积为2.24L。选项为D。
本题难度:一般
2、简答题 钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.V2O5是接触法制硫酸的催化剂.
(1)一定条件下,SO2?与空气反应t?min后,SO2?和SO3物质的量浓度分别为a?mol/L、b?mol/L,则SO2?起始物质的量浓度为______mol/L;生成SO3的化学反应速率为______.
(2)全钒液流储能电池是利用不同价态离子对,发生氧化还原反应来实现化学能和电能相互转化的,其装置原理如图:
①当左槽溶液逐渐由黄变蓝,其电极反应式为______.
②充电过程中,右槽溶液颜色逐渐由______色变为______色.
③充电时若转移的电子数为3.01×1024个,左槽溶液中n(H+)的变化量为______?mol.
参考答案:(1)2SO2+O2
本题解析:
本题难度:一般
3、填空题 某化学兴趣小组进行如下图所示的电化学实验,实验前查资料获知:铁氰化钾(K3[Fe(CN)6])遇Fe2+产生 蓝色沉淀。V形管以多孔Pt为电极;U形管A端滴入1~2滴K3[Fe(CN)6]溶液。
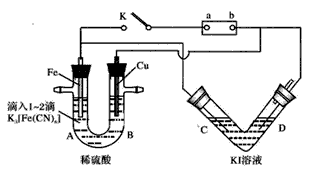
(1)开始时,接通K电键:U形管中无沉淀,却观察到B端____;根据以上实验可知电源正极为____(填“a”或“b”)。Fe电极上发生的电极反应为___,V形管中现象是___ 。
(2)断开K电键,U形管中现象:A端___;B端____,B端有关反应方程式为____。V形管中现象与(1)的____(填“相同”或“不同”)。
参考答案:(1)溶液变蓝色; b; 2H++2e-==H2↑ ;C端产
本题解析:
本题难度:一般
4、填空题 (16分)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,
总反应为:2CH3CHO + H2O ="==" CH3CH2OH + CH3COOH。实验室中,以一定浓度的乙醛―Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。

(1)若以甲醇燃料电池为该电解的直流电源,燃料电池中的电解液是氢氧化钠溶液,则燃料电池中b极的电极反应式为 。电池工作一段时间后,氢氧化钠溶液物质的量浓度 (填变大,变小或不变)
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。阳极电极反应如下:① 4OH- - 4e-="=" O2↑+ 2H2O;②
(3)已知:乙醛、乙醇的沸点分别为20.8℃、78.4℃。从电解后阴极区的溶液中分离出乙醇粗品的方法是 。
(4)若直流电源使用新型的熔融碳酸盐燃料电池(MCFS),该电池以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650 ℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1∶1)直接作燃料,其工作原理如图所示。

①B极发生______(填“氧化”或“还原”)反应,电极反应式 。
②以此电池电解足量的CuSO4溶液,当电池消耗1.12L(标准状况下)氧气时,则阴极产物的质量为_ _____ g。加入一定量的 可以让CuSO4溶液回复原状。
A、CuO B、Cu(OH)2 C、CuCO3 D、Cu
参考答案:(1)CH4O-6e- +8 OH- ="=" CO32-+
本题解析:
试题解析:(1)由图示可知,a连阳极,b连阴极,所以b为负极,若以甲醇燃料电池为该电解的直流电源,燃料电池中的电解液是氢氧化钠溶液,则燃料电池中b极的电极反应式为CH4O-6e- +8 OH- ="=" CO32-+6H2O,由电极反应可得,氢氧化钠参与反应,电池工作一段时间后,氢氧化钠溶液物质的量浓度变小;(2)阳极发生氧化反应,生成乙酸和氧气,电极反应为CH3CHO-2e-+H2O
本题难度:困难
5、选择题 500mLKNO3和Cu(NO3)2的混合溶液中c(NO3-)=6mol?L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
A.原混合溶液中c(K+)为4mol?L-1
B.上述电解过程中共转移4mol电子
C.电解得到的Cu的物质的量为0.5mol
D.电解后溶液中c(H+)为2mol?L-1
参考答案:石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4
本题解析:
本题难度:一般
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
|
 2Cu + 2H2SO4+ O2↑.在整个闭合回路中电子转移数目相等。所以n(Cu)=12.8g÷64g/mol=0.2mol.n(e-)=0.4mol。所以n(O2)=0.1mol.在标准状况下其体积为2.24L。选项为D。
2Cu + 2H2SO4+ O2↑.在整个闭合回路中电子转移数目相等。所以n(Cu)=12.8g÷64g/mol=0.2mol.n(e-)=0.4mol。所以n(O2)=0.1mol.在标准状况下其体积为2.24L。选项为D。
