时间:2017-01-24 19:00:28
1、实验题 下列实验操作或对实验事实的描述正确的是?????????????(填序号)
①仅用蒸馏水可鉴别出蔗糖、硫酸铜、碳酸钙三种粉末;
②实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉;
③配制一定浓度的溶液时,俯视容量瓶的刻线,会使配制的浓度偏低;
④用瓷坩埚熔化各种钠的化合物;
⑤分液时,先从分液漏斗中倒出上层液体,后放出下层液体;
⑥测溶液大致的pH:用玻璃棒蘸取溶液滴在湿润的pH试纸上,与标准比色卡对照;
⑦向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水现象相同;
⑧分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积前者少,后者多。
参考答案:
①②⑦⑧
本题解析:
配制一定浓度的溶液时,俯视容量瓶的刻线,体积偏小,导致浓度偏大,③错误;瓷坩埚的主要成分为SiO2,能够与一些钠的化合物反应,如NaOH、Na2CO3等,所以应该用铁坩埚,④错误;分液时,上层液体从分液漏斗上口倒出,下层液体从下端放出,⑤错误;测溶液pH时,试纸不能湿润,否则溶液稀释,可能导致pH变化,⑥错误。
本题难度:一般
2、实验题 某校研究性学习小组同学在实验时把一定量的SO2通入装有一定浓度BaCl2溶液的试管中,出现了白色浑浊物。
⑴实验小组的同学查阅了工具书上的相关数据,经过计算推导得出:即使把SO2通入BaCl2溶液中至饱和,也不可能生成BaSO3,故白色浑浊物只能是BaSO4。你认为所查阅的数据为:
SO2的溶解度、SO2饱和溶液中各离子的浓度以及_______________。
⑵小组同学对白色浑浊物成分及产生原因进行了各种合理的假设,并分别设计实验验证假设如下: 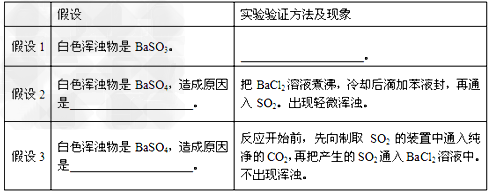
请把上表填充完全。
⑶写出在验证假设2的实验时,溶液中发生的反应的化学方程式:________________、
_______________;
⑷请你再提供一种假设。白色浑浊物是BaSO4,造成原因是________________。
参考答案:⑴BaSO3的溶度积或BaSO3的溶解度???
⑵假设
本题解析:
本题难度:一般
3、选择题 下列实验能获得成功的是(???)
A.苯和浓溴水用Fe作催化剂制溴苯
B.氯乙烷与NaOH溶液共热,水解后加入AgNO3溶液检验Cl-
C.CH4和Cl2光照制得纯净的CH3Cl
D.乙烯通入含Br2的CCl4溶液制得CH2BrCH2Br
参考答案:D
本题解析:略
本题难度:简单
4、实验题 为研究铁质材料与热的浓硫酸的反应,某小组进行了以下探究活动:
【探究一】
(1)称取铁钉(碳索钢)12. 0 g放入30. 0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除含有Fe3+外还可能有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为
_______(选填序号);
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应SO2+Br2+2H2O =2HBr+H2SO4,然后 加入足量BaCl2溶液,得到4.66g沉淀,据此推知气体Y 中SO2的体积分数为_____________
【探究二】
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和CO2。为此设计了下列探究实验装置(图中央持仪器省略)。 
(2)写出产生CO2的化学方程式____________________
(3)装置A中试剂的作用是_________________
(4)简述确认气体Y中含有CO2的实验现象:____________________
(5)如果气体Y中含有H2,预计实验现象应是:______________________
参考答案:(1)①d;②66.7%(或2/3)
(2)C+2H
本题解析:
本题难度:一般
5、实验题 某研究性学习小组利用H2还原法测定两种铜的氧化物CuO、Cu2O混合粉末中铜元素的质量分数。下图是测定装置的示意图,A中的试剂是盐酸。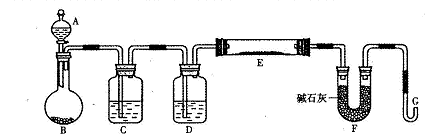
请回答下列问题。
(1)烧瓶中装入的试剂是锌粒,其中将发生反应的离子方程式是??????????????????;
(2)试剂C是水,其作用是__?????????????????__;
(3)试剂D是__???????????__,其作用是干燥氢气;
(4)连接好装置后的实验操作依次是_??????????__(填下列操作序号)
①检验氢气纯度;②加热E;③检验装置气密性;④点燃G管溢出的气体;⑤从A瓶逐滴滴加液体
(5)已知:C(s)+1/2O2( g)= CO(g)??△H=-110.5kJ・mol-1,
Cu2O(s) +1/2O2(g) = 2CuO(s)??△H=-145 kJ・mol-1
则用炭粉在高温条件下还原CuO生成Cu2O的热化学方程式:____??????????????。??
参考答案:(1)Zn + 2H+= Zn2+ + H2↑ (1分) 本题解析: 本题难度:一般
试题分析:A、B装置是氢气的发生装置,C装置是除杂装置,目的是除去氢气中的HCl气体,D装置是干燥装置,E是反应装置,碱石灰是吸收生成的水,G
(4)收集或进 行气体实验时,应在装入药品前先进行气密性的检查。点燃可燃性气体(如H2、CO、CH4、C2H2、C2H4等)之前,或用CO、H2还原Fe2O3、CuO之前,要检验气体纯度,能点燃G管溢出的气体,说明氢气充满了整个装置,然后再加热E,不会发生危险。
(5)热化学方程式的合并。由第一个方程式减去第二个方程式即可得到目标方程式。