时间:2017-01-24 18:54:15
1、选择题 下列装置可以构成原电池的是 [???? ]
A.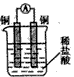
B.
C.
D.
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列说法正确的是( )
A.钢铁发生电化学腐蚀的正极反应式:Fe═Fe2++2e-
B.氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH-
C.粗铜精炼时,与电源正极相连的是纯铜
D.在铁上镀铜时,可用CuSO4溶液作为电解液
参考答案:A.钢铁的电化学腐蚀中,负极上电极反应式为:Fe-2e-═F
本题解析:
本题难度:一般
3、选择题 下列关于原电池的叙述不正确的是
A.原电池是将化学能转化为电能的装置
B.原电池中电子流入的一极是正极,发生氧化反应
C.在氢—氧燃料电池中通入H2的一极是负极
D.把铜片和锌片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
参考答案:B
本题解析:A 正确,原电池就是将化学能转化为电能的装置
B 错误,正极发生还原反应。
C 正确,在氢—氧燃料电池中通入H2的一极失去电子,为负极。
D 正确,铜片是正极,溶液中的氢离子向正极移动,得电子生成氢气,所以,铜片表面出现气泡。
本题难度:一般
4、简答题 在铜-锌原电池中,理论上应观察到的现象是:铜片上:______锌片上:______.此时原电池的电极反应式是:正极:______负极:______.但在实际实验中,锌片上也有______、表面变黑等现象,其原因是______.
在相同温度下,同样大小的混有碳粒等杂质的锌比纯锌与同浓度同体积的稀硫酸反应的速率______(选填“要快”、“要慢”、“相等”、“无法确定”),其微观解释是______.
参考答案:该原电池中,铜片上,氢离子得电子生成氢气,所以看到的现象是:
本题解析:
本题难度:一般
5、选择题 在下图所示的原电池中,正极发生的反应是(???)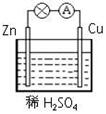
A.H2-2e- ==2H+
B.Cu-2e- ="=" Cu2+
C.2H+ + 2e- ="=" H2↑
D.Zn-2e- ="=" Zn2+
参考答案:C
本题解析:略
本题难度:简单