时间:2017-01-19 12:18:12
1、选择题 下列四个反应可用H++OH-=H2O这个离子方程式表示的是(???)
A.Ba(OH)2溶液与稀硫酸
B.Cu(OH)2与稀硫酸
C.NaOH溶液与稀硫酸
D.NH3?H2O与稀硫酸
参考答案:C
本题解析:
试题分析:A不正确,因为反应中还有硫酸钡白色沉淀生成;B不正确,氢氧化铜是难溶性物质,应该用化学式表示;D不正确,氨水是弱碱,应该用化学式表示,因此正确的答案选C。
点评:该题是中等难度的试题,属于离子方程式的逆向判断,有利于培养学生的逻辑推理能力和逆向思维能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:简单
2、选择题 某溶液只可能含有?Na+、Ag+、Al3+、AlO2-、S2-、CO32-、SO32-、NO3-等离子中的数种.向此溶液中加入稀盐酸,溶液变浑浊并有气体出现.根据上述现象,判断下列结论中不正确的是
A.此溶液中一定有Na+、S2-、SO32-
B.此溶液中可能有AlO2-、CO32-
C.此溶液中一定没有Ag+、Al3+
D.此溶液中可能有S2-、NO3-
参考答案:A
本题解析:分析:溶液中加入稀盐酸,溶液变浑浊并有气体出现,浑浊现象可能是Ag+、AlO2-作用生成AgCl、Al(OH)3沉淀,NO3-,S2-存在加入盐酸可以出现沉淀硫;出现气体可能是S2-、CO32-、SO32-离子结合氢离子生成硫化氢气体、二氧化碳气体、二氧化硫气体;所以推断一定不含银离子,若含有银离子,则S2-、CO32-、SO32-离子都不能存在,判断一定含有AlO2-,依据离子共存判断Al3+一定不存在,溶液中一定含有钠离子,AlO2-离子,S2-、CO32-、SO32-、NO3-离子可能含有.
解答:溶液中加入稀盐酸,溶液变浑浊并有气体出现,浑浊现象可能是Ag+、AlO2-作用生成AgCl、Al(OH)3沉淀,NO3-,S2-存在加入盐酸可以出现沉淀硫;出现气体可能是S2-、CO32-、SO32-离子结合氢离子生成硫化氢气体、二氧化碳气体、二氧化硫气体;所以推断一定不含银离子,若含有银离子,则S2-、CO32-、SO32-离子都不能存在,判断一定含有AlO2-,依据离子共存判断Al3+一定不存在,溶液中一定含有钠离子,AlO2-离子,S2-、CO32-、SO32-、NO3-离子可能含有;
A、此溶液中一定有Na+,S2-、SO32-离子不一定都含有,故A错误;
B、此溶液中可能有AlO2-、CO32-,依据分析判断,结论正确,故B正确;
C、上述分析判断可知,此溶液中一定没有Ag+、Al3+,故C正确;
D、上述分析判断可知,此溶液中可能有S2-、NO3-,故D正确;
故选A.
点评:本题考查了离子性质的应用和离子检验方法的分析判断,掌握离子性质的反应现象是解题关键,题目难度较大.
本题难度:一般
3、选择题 NaHCO3和NaHSO4两溶液混合后,实际参加反应的离子是[???? ]
A.H+和CO32-
B.CO32-和HSO4-
C.Na+、CO32-和H+
D.HCO3-和H+
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列各组无色溶液的离子组在pH=l时能大量共存的是
A.NH4+、Cl-、Mg2+、SO42-
B.Al3+、Cu2+、SO42-、Cl-
C.Ba2+、K+、NO3-、OH-
D.Ca2+、Na+、Cl-、AlO2-
参考答案:A
本题解析:
本题难度:简单
5、填空题 某溶液中可能含有H+、Na+、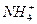 、Mg2+、Fe3+、Al3+、
、Mg2+、Fe3+、Al3+、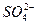 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_____________,且各阳离子的物质的量之比为_____________;肯定不含有的阳离子是_____________;检验可能含有的某种阳离子的实验方法是____________________________________________________。
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_____________,且各阳离子的物质的量之比为_____________;肯定不含有的阳离子是_____________;检验可能含有的某种阳离子的实验方法是____________________________________________________。
参考答案:H+、Al3+、本题解析:由图可知,由于起始时加入NaOH时没有沉淀生成,所以溶液中肯定含有H+,且物质的量可以设为2 mol;由于沉淀最终随着NaOH的加入完全消失,所以溶液中肯定不含Mg2+、Fe3+,肯定含有Al3+,物质的量为1 mol;根据图象中的平行线可知溶液中含有
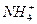 ,且物质的量为3 mol。所以溶液中各阳离子的物质的量之比为
,且物质的量为3 mol。所以溶液中各阳离子的物质的量之比为
本题难度:简单