时间:2017-01-19 11:55:55
1、选择题 利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池。
(1)负极材料是________(写名称),电极反应为__________________。
(2)正极电极反应式为__________________________________。
(3)溶液中SO42—向________极移动。
参考答案:(1)铜 Cu-2e-=Cu2+ (2)O2+4e-+4H+
本题解析:该氧化还原反应中还原剂为Cu,故负极是铜,电极反应为Cu-2e-=Cu2+,氧化剂是O2,故正极反应为O2+4e-+4H+=2H2O,溶液中阴离子SO42—向负极移动。
本题难度:一般
2、选择题 如图所示的装置能够组成原电池产生电流的是( )
A.
稀硫酸钠
B.
NaCl溶液
C.
D.
酒精
参考答案:A.两个电极材料相同,不能够组成原电池且产生电流,故A错误;
本题解析:
本题难度:简单
3、选择题 某小组为研究电化学原理,设计了下图所示的电化学装置,电极I为锌,其他电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液。下列叙述正确的是
A.电子由电极IV通过外电路流向电极I
B.装置工作过程中III电极周围出现红色
C.电极II发生还原反应
D.盐桥中Cl—向乙池移动
参考答案:C
本题解析:
试题分析:该图所示的电化学装置其实是以甲乙和盐桥形成原电池并以该原电池为电源形成丙电解池。电极I是负极、电极II是正极、电极III是阳极、电极IV是阴极。A、甲是原电池,电极I为锌,作负极,电子由负极I通过外电路流向阴极IV, A错误;B、装置工作过程中作为阳极的III电极Cl—失去电子产生氯气,电极周围不出现红色, B错误;C、电极II为原电池的正极Cu2+离子在这里得电子被还原,发生还原反应,C正确;D、原电池中阴离子向负极移动,故盐桥中Cl—向甲池移动,D错误。答案选C。
考点:考查原电池、电解池装置及原理。
本题难度:一般
4、选择题 X、Y、Z三种金属,X、Y组成原电池,X是负极;把Y放在Z的硝酸银溶液中,Y表面有Z析出。其活泼顺序是
A.X>Y>Z
B.Z>Y>X
C.X>Z>Y
D.Y>X>Z
参考答案:A
本题解析:
试题分析:原电池中较活泼的金属做负极,X、Y组成原电池,X是负极,则金属性是X大于Y;活泼的金属能置换出不活泼的金属,所以把Y放在Z的硝酸银溶液中,Y表面有Z析出,说明金属性是Y大于Z,所以X、Y、Z三种金属的活泼性是X>Y>Z,答案选A。
点评:该题是高考中的常见考点,属于基础性试题的考查,难度不大。明确金属性强弱比较的判断依据,是答题的关键,有利于培养学生的逻辑推理能力。
本题难度:简单
5、选择题 如图是一种染料敏化太阳能电池的示意图。电池的一个电极由有机光敏燃料(S)涂覆在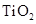 纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为: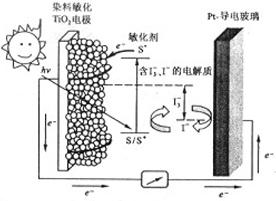
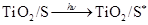 (激发态)
(激发态)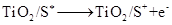
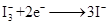
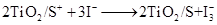
下列关于该电池叙述错误的是:
A.电池工作时,是将太阳能转化为电能
B.电池工作时,I-离子在镀铂导电玻璃电极上放电
C.电池中镀铂导电玻璃为正极
D.电池的电解质溶液中I-和I3-的浓度不会减少
参考答案:B
本题解析:
试题分析:由图电子的移动方向可知,半导材料TiO2与染料为原电池的负极,铂电极为原电池的正极,电解质为I3-和I-的混合物,I3-在正极上得电子被还原,正极反应为I3-+2e-=3I-。由图电子的移动方向可知,半导材料TiO2与染料为原电池的负极,铂电极为原电池的正极,电解质为I3-和I-的混合物,I3-在正极上得电子被还原,正极反应为I3-+2e-=3I-,A、该电池是将太阳能转化为电能的装置,故A正确;B、电池工作时,I-离子在铂电极上放电,发生氧化反应,故B错误;C、电池工作时,I3-到Pt
本题难度:一般