A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
C.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.c(OH-)>c(H+)>c(Cl-)>c(NH4+)
参考答案:CD
本题解析:
本题难度:一般
3、填空题
在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH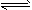 CH3COO-+H+ △H>0
CH3COO-+H+ △H>0
(1)下列方法中,可以使0.10mol·L-1 CH3COOH溶液中CH3COOH电离程度增大的是____________。
a.加入少量0.10mol·L-1的稀盐酸 b.加热CH3COOHc.加入稀释至0.010mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10mol·L-1的NaOH溶液
(2)25℃时,该电离平衡的平衡为1.75×10-5。现有:
①0.100.010mol·L-1 CH3COOH溶液 ②0.00100.010mol·L-1 CH3COOH溶液 其c(H+)之比为①:②=______。(提示:进行简化计算,平衡时的c(CH3COOH)可用起始浓度代替,水电离出的c(H+)、c(OH-)忽略不计,下同)
(3)25℃时,向0.10mol·L-1 CH3COOH溶液中加入一定量固体CH3COONa(假设溶液体积不变),若溶液中c(CH3COO-)为1.0mol·L-1,则溶液中c(H+)=________mol·L-1 (计算结果保留小数点后两位有效数字)。溶液中各种离子浓度关系是_________。
参考答案:(1)bcf
(2)10:1
(3)c(CH
本题解析:
本题难度:一般
4、选择题 化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是
 [???? ]
[???? ]
A.根据图①可判断可逆反应“A2(g)+3B2(g)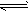 2AB3(g)”的ΔH>0
2AB3(g)”的ΔH>0
B.图②表示压强对可逆反应2A(g)+2B(g)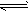 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO,至pH在4左右
参考答案:D
本题解析:
本题难度:一般
5、简答题 某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验以下实验:将pH═2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
(1)HA为______酸,HB为______酸;(填“强“或“弱“)
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为______(用酸、碱化学式表示);将稀释后的HA溶液利MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为______;(填“大于“、“小于“或“等于“)
(3)若b+c=14,则MQH为______碱(填“强“或“弱“).将稀释后的HB溶液和MOH溶液取等体积混合,所得很合溶液的pH______7(填“大于“、“小于“或“等于“)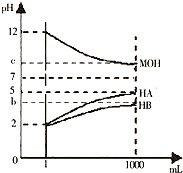
参考答案:(1)由图可知,pH═2的两种酸溶液HA,HB各1mL,分别
本题解析:
本题难度:一般