时间:2017-01-19 10:29:27
1、选择题 .常温下,向20?mL?0.2?mol/L?H2A溶液中滴加0.2?mol/L ??NaOH溶液。有关微粒的物质的量变化如图(其中I代表 ??H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是???????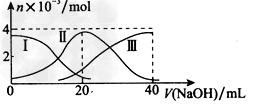 [???? ]
[???? ]
A.当V(?NaOH)=20??mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)??
B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 ??
C.欲使NaHA溶液呈中性,可以向其中加入酸或碱 ??
D.向NaHA溶液加入水的过程中,pH可能增大也可能减小
参考答案:A
本题解析:
本题难度:一般
2、选择题 实验测得常温下0.1mol/L某一元酸(HA)溶液的pH不等于l, 0.1mol/L某一元碱(BOH)溶液里:
c(H+)/c(OH-)=10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是 [???? ]
A.c(A-)>c(B+)>c(H+)>c(OH-)
B.c(B+)>c(A-)>c(OH-)>c(H+)
C.c(B+)+c(H+)>c(A-)+c(OH-)
D.c(B+)>c(A-)>c(H+)>c(OH-)
参考答案:B
本题解析:
本题难度:一般
3、选择题 常温下,将amol/L的MOH(可溶性弱碱)与bmol/L的盐酸等体积混合,已知相同条件下MOH的电离程度大于M+的水解程度,则下列有关推论不正确的是??[???? ]
A.若混合后溶液的pH=7,则c(M+)=c(Cl-) ????
B.若a=2b,则c?(M+)?>?c(Cl-)?>?c?(MOH)?>?c(OH-)?>?c(H+) ????
C.若b=2a,则c(Cl-)?>?c(M+)?>?c(H+)?>?c(OH-)? ????
D.若混合后溶液满足c(H+)=c(OH-)+c(MOH),则可推出a=b
参考答案:C
本题解析:
本题难度:一般
4、选择题 25℃时,在25mL?0.1mol?L-1的NaOH溶液中,逐滴加入0.2mol?L-1的CH3COOH溶液,溶液的pH与醋酸体积关系如图,下列分析正确的是( ? )