ʱ��:2017-01-19 10:22:14
1������� ��֪A��B��C��Ϊ�����ĵ��ʣ�����AΪ������B��CΪ�ǽ�������һ���������ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ�����ʡ�ԣ�
��ش�
��1����������B��C��Ϊ���壬DΪ��ɫ���壬E�ĵ���ʽΪ______��A��E��һ�������·�Ӧ����D�Ļ�ѧ����ʽΪ______��
��2����������BΪ���壬CΪ��ɫ���壬�ɽ���A��ԭ�ӽṹʾ��ͼΪ______��E�ĽṹʽΪ______��A��E��һ�������·�Ӧ����D�Ļ�ѧ����ʽΪ______��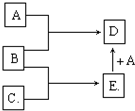
�ο��𰸣���1��B��CΪ��̬�ǽ�������Χ��С����������A����������Ӧ��
���������
�����Ѷȣ�һ��
2������� ��ȸʯ��Ҫ��Cu2��OH��2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4?5H2O��CaCO3���������£�
�Իش��������⣺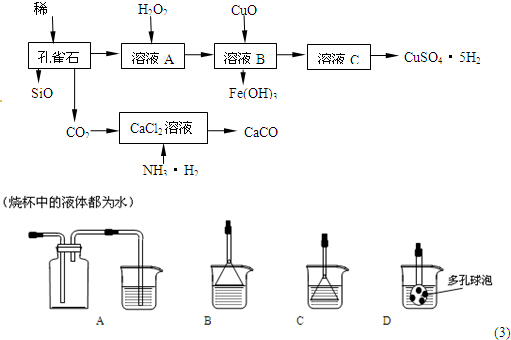
��1����δ����H2O2����ҺA�У����ڵĽ���������Cu2+��Fe2+��Fe3+�����������Һ��Fe3+��ѡ������ʵ��Լ���______������ţ���
A��KMnO4��Һ������B��Fe��????????C��?Na2CO3��Һ???????D��KSCN��Һ
����ҺA�м���H2O2��H2O2�ڸ÷�Ӧ������������ʵ����ѡ��H2O2������Cl2���������������ǻ��������⣬��һԭ���Dz���������______���ӣ�
��2������ҺC���CuSO4?5H2O����Ҫ��������Ũ����______�����˵Ȳ��������ձ���©���⣬���˲��������õ���һ�����������������ڴ˲����е���Ҫ������______��
��3���Ʊ�CaCO3ʱ��������Ӧ�Ļ�ѧ����ʽ��______����ʵ��������а����ݳ�����ѡ������װ���е�______������ţ�װ�����հ�����
��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ�������100mL?0.1mol�MLKMnO4����Һ�����Ƹ���Һʱ�����ձ�������������ͷ�ι��⣬�����һ�ֲ���������______�������ò��������м�����ˮ���ӽ��̶���1-2cmʱ��Ӧ����______�μ�����ˮ����Һ�İ�Һ��������̶�����ƽ��
�ο��𰸣���1����������Һ��Fe3+��ʹ�õ��Լ���KSCN��Һ����Һ��
���������
�����Ѷȣ�һ��
3������� ��֪A����H������ת����ϵ
��1����A��Ӧ��������ƣ�?????????????????????????????????
��2��д��Eת���F�Ļ�ѧ����ʽ��??????????????????????????
��3��д��D��AgNO3��Һ��Ӧ�Ļ�ѧ����ʽ��?????????????????????????
��4��д��G��Һ��A��Ӧ�����ӷ���ʽ?????????????????????
��5������G��Һ���õ��Լ��ǣ�???????????????????????
�ο��𰸣���1������(д��HCl������)???????��2��4Fe(O
�����������ɫ����E�ɱ�����Ϊ����ɫ����F����֪EΪFe(OH)2��FΪFe(OH)3��F�������к�����GΪFeCl3
D��Һ�������ữ����������Һ�ɵõ���ɫ��������ɫ��Ӧ����ɫ����Һ�����֪D��Һ�к���Cl����K+����DΪKCl
��B+C��Fe(OH)2+KCl��֪B��C����һ����ΪFeCl2����һ����ΪKOH�����B����A��Ӧ����G��FeCl3�������ж�BΪFeCl2��CΪKOH��AΪ��
�������ᣨB��Һ������FeCl2������
�����Ѷȣ�һ��
4������� (15��)�Ķ��������ϣ��ݴ��������Ҫ��
������Ԫ��A��B��C��D��E��F�����ǵ�ԭ������������������B��CΪͬһ���ڣ�D��E��FΪͬһ���ڣ�A��D��C��F�ֱ�Ϊͬһ���壻CԪ��ԭ�ӵ������������Ǵ�����������3����D����������ԭ�Ӱ뾶����Ԫ��(��ϡ��������)��E�Ƿǽ���Ԫ�أ��䵥���ڵ��ӹ�ҵ������Ҫ�ô���
��AԪ����̼Ԫ�ذ�������1��3�����γɻ�����X����C2��X��23.4gD2C2�����ܱ������У��õ������ѧ��Ӧ����Ӧ�����������ڵ���ѹΪ��(250��)��������������ˮ�У��������������C2��X�����ʵ���֮��Ϊ???????�������䷴Ӧ����ʽ����������Ӧ����4mol����ת�ƣ�������C2�����ʵ���Ϊ???????mol��
�ƹ�ҵ����������E�Ļ�ѧ����ʽΪ��????????????????????????????��ָ��E����������ͨѶ�е�һ����;????????????????????????????��
��һ�������£�A2������B2�����ַ�Ӧ������6.8g�ռ乹�������ε����壬�ų�18.44kJ��������÷�Ӧ���Ȼ�ѧ����ʽΪΪ��????????????????????????��A��B��ԭ�Ӹ�����1��2���γ����ԭ������Ϊ32�Ļ����д���û��������������ᷴӦ�����ӷ���ʽ???????????????????????????????��
��A2��C2��KOH��Ũ��Һ�п����γ�ԭ��ء������PtΪ�缫���ڵ�ص������ֱ�ͨ��A2��C2����ͨ���A2һ���ĵ缫��ӦʽΪ��?????????????????????????????��
����10L���ܱ������У�ͨ��2molFC2��3molC2���壬һ�������·�Ӧ������FC3���壬����Ӧ�ﵽƽ��ʱ��C2��Ũ��Ϊ0.21mol/L����ƽ��ʱFC2��ת����Ϊ?????????????��
�ο��𰸣�(15��)������������Ƴ�A��B��C��D��E��F�ֱ�Ϊ��H��N��O��Na��Si��S��XΪ���飬������ӦΪ��2CH4+O2+6Na2O2=2Na2CO3+8NaOH,�ʣ�1���������3��������5����
�����Ѷȣ���
5��ѡ���� A��һ�ֳ����ĵ��ʣ�B��CΪ��ѧ�����Ļ����A��B��C������Ԫ��X.��������ͼ��ʾ��ת����ϵ(���ֲ��P��Ӧ��������ȥ)�������ж���ȷ����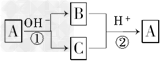 [???? ]
[???? ]
A��XԪ�ؿ���ΪAl
B��XԪ�ؿ����ǽ�����Ҳ�����Ƿǽ���
C����Ӧ�ٺ͢ڻ�Ϊ���淴Ӧ
D����Ӧ�ٺ͢�һ��Ϊ������ԭ��Ӧ
�ο��𰸣�D
���������
�����Ѷȣ�һ��