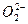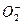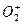D
性质或结构信息
室温下单质呈粉末状固体,加热易熔化;单质在氧气中燃烧发出明亮的蓝紫色火焰
单质在常温、常压下是气体,能溶于水;原子的M层比L层少1个电子
单质为质软、银白色固体,导电性强;单质在空气中燃烧发出黄色火焰
原子的最外电子层上电子数比内层电子总数少6;单质为空间网状晶体,具有很高的熔沸点
(1)B在元素周期表中的位置是第______周期______族,写出A原子的原子结构示意图:______.
(2)写出C单质与水反应的化学方程式:______.A与C形成的化合物溶于水后,溶液的pH______7(填“大于”、“等于”或“小于”).
(3)D的最高价氧化物晶体的硬度______(填“大”或“小”),其理由是______.
(4)A、B两元素非金属性较强的是(写元素符号)______;写出能证明这一结论的实验事实:______.
参考答案:A、B、C、D四种短周期元素:室温下A的单质呈粉末状固体,加
本题解析:
本题难度:一般
4、选择题 下列表示物质结构的化学用语或模型正确的是[???? ]
A.8个中子的碳原子的符号:12C
B.NaCl的电子式: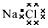
C.Cl-的结构示意图:
D.CH4分子的比例模型:
参考答案:D
本题解析:
本题难度:简单
5、填空题 从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质.
(1)下列说法正确的是?????????(填字母).
A.元素电负性由大到小的顺序为F>O>N
B.一个苯分子含3个π键和6个σ键
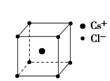
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小为Br>Se>As
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为?????????.光气(COCl2)各原子最外层都满足8电子稳定结构,COCl2分子空间构型为?????????(用文字描述).
(3)Cu 2+基态的电子排布式为?????????.向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4晶体,该物质中配位原子的杂化方式为?????????,不考虑空间构型,其内界结构可用示意图表示为?????????.
参考答案:(1)A ;(2)OCS?平面三角形
(3)1s22s
本题解析:(1)A.同周期自左而右电负性增大,故电负性F>O>N,故A正确;
B.苯分子中化学键是介于单键与双键之间的一种特殊化学键,故B错误;
C.氯化钠晶体中氯离子配位数为6、氯化铯晶体中氯离子的配位数为8,故D错误;
D.同周期自左而右等于电离能呈增大趋势,但As原子4p能级有3个电子,处于半满稳定状态,能量降低,第一电离能高于同周期相邻元素,故第一电离能Br>As>Se,故D错误;
故选:A;
(2)羰基硫(OCS)与CO2为等电子体,具有CO2分子结构,故羰基硫(OCS)结构
本题难度:一般
|